表型筛选的进展:药物发现的转折点?

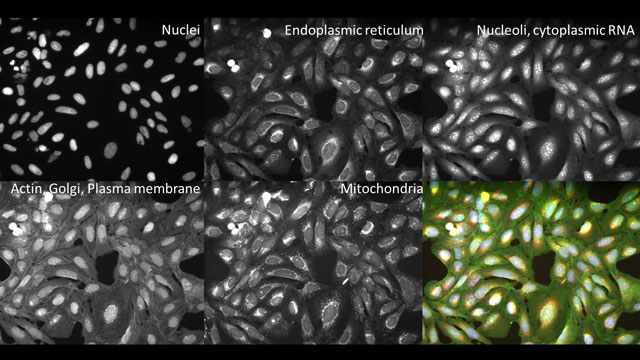
拓扑异构酶抑制剂和蛋白激酶ATR抑制剂治疗人类结直肠癌细胞。细胞核(蓝色),DNA损伤(红色),DNA复制焦点(绿色)。来源:Yves Pommier, Rozenn Josse, NCI癌症研究中心。
阅读时间:
药物发现方法大致可分为两类:基于靶标的方法和基于靶标的方法表型筛选.从历史上看,药物的选择是根据其可见(或可感知)的健康益处,系统的表型分析在20世纪初开始受到关注。到20世纪90年代末,基于靶标的药物发现在分子生物学几十年的进步基础上主导了制药业。
今天,它很容易被发现不满药物发现成功率;尽管取得了重大的技术进步,医药研发投入也在不断增加,但这一趋势一直在稳步推进下降在新药进入临床开发和进入市场的数量上。从2006年到2015年,从I期进展到美国FDA批准的总体可能性仅为9.6%生物的报告临床开发成功率(n = 9985)。虽然转向基于靶标的药物发现并不是这种低效率的唯一解释,但有一个原因共识我们过于依赖于假设目标或途径与疾病之间的联系β淀粉样蛋白假设就是一个经典的例子)。
在基于靶标和表型的药物发现方法之间的选择并不是一个“非此即彼”的问题,因为现实是介于混乱的中间。然而,现在迫切需要将承认生物系统复杂性的研究模型和技术结合起来。在本文中,我们探讨了与基于细胞的表型筛选相关的最新发展,讨论了良好的表型药物筛选的要素,并发现这些方法如何帮助为药物筛选提供更准确的生物学背景。
什么是基于细胞的表型筛查?
在药物发现的背景下,基于细胞的表型测定是一种化合物筛选系统,以一种与疾病具有生物学相关性的方式,专注于细胞表型的调节。虽然表型筛选主要用于化合物筛选,但它也用于一般研究——例如,研究基因敲除和过表达,或比较个体患者样本。最纯粹的形式,表型筛选识别产生理想生物效应的化合物,而不需要事先知道它们对特定目标的活性或作用方式。在实践中,表型筛选项目并不总是与目标无关,布罗德研究所的一位高级计算生物学家说,Beth Cimini博士“这是一个范围;你可以有一个也有表型成分的目标分析,你可以有一个纯粹专注于目标的分析,或者你可以有一个根本没有目标的分析。”
研究人员希望表型筛选能够更好地预测具有治疗价值的化合物,因为可以在模拟疾病某些方面的基于细胞(或组织或整个生物体)的模型中观察到相关的和可测量的变化。表型药物筛选利用核染料、免疫组织化学和其他工具来观察表型变化,如与细胞形态(包括细胞核或其他细胞器)、空间排列(模式和间距)、特定蛋白质/s的产生、基因表达或细胞死亡有关的变化。有时,疾病的特征不符合表型,可以很容易地筛选和潜在的分子事件被用作代理人.
是什么造就了一个好的表现型药物筛选?
从根本上说,良好的表型药物筛选最重要的特征是其可翻译性,即筛选分析预测药物临床治疗反应的能力。但这在实践中意味着什么呢?在深入投入临床试验之前,我们如何知道表现型药物筛选是否是一种好方法?在2015年,文森特等人。提出了表型筛选“3规则”,并强调了三个具体标准,以帮助设计最具预测性的表型分析:
- 系统:该检测与疾病的相关性如何?这些细胞适合做实验吗?
- 刺激因素:刺激因素与疾病的相关性如何?理想情况下,表型分析将使用高度相关的细胞,例如包含致病基因改变的患者来源细胞。如果这是不可能的,“最好的猜测”的努力,如使用炎症或细胞毒性药物来重建细胞损伤的兴趣。
- 终点:检测结果与临床终点的关系如何?使用小型化的临床终点作为检测读数的检测比那些不接近复制关键的检测更受欢迎在活的有机体内疾病表型。
患者来源的类器官给个性化医疗带来了希望
为了解决对更复杂的细胞模型的需求,以便更好地概括在活的有机体内生理学上,一系列的微生理系统已经出现。与二维单层细胞相比,microphysiological系统可以具有关键的生物刺激,包括机械线索(如剪切应力和拉伸),三维微环境,持续的浓度梯度,以及多种细胞类型之间的相互作用。这些系统(被描述为芯片上的器官、类器官、3D球体和静态微图案技术)使用微工程技术、药物输送和/或传感工具来检查药物和/或微环境对活细胞的影响。人类瀑样是三维多细胞的在体外作为药物发现和人类特异性疾病机制研究工具的组织结构。它们受到青睐,因为它们至少能够模仿器官的某些功能,并且可以从诱导多能干细胞或供体组织中获得。
肠道瀑样由直肠活检已被用于研究遗传性疾病,如囊性纤维化。在荷兰Hubrecht研究所的Clevers实验室,研究人员一直在寻找一种侵入性较小的类器官发育方法。利用在囊性纤维化患者尿液中发现的肾源细胞,Schutgens等人(2019)报告原发性肾小管上皮类器官的发育,称为“小管”,代表近端和远端肾单元段。在囊性纤维化中,基因突变雌性生殖道(囊性纤维化跨膜传导调节因子)基因损害离子和液体在一系列上皮中的运输功能。为了证明小管的适用性体外评估治疗效果,分组完成了福斯克林溶胀试验.
Clevers实验室的博士生Maarten Geurts解释了该检测如何用于评估类器官中的药物反应:“将Forskolin添加到健康的肠道类器官中会在一小时内产生(cftr依赖的)肿胀反应,而在cf患者衍生的类器官中则没有这种反应。在类器官中加入福斯克林诱导的肿胀反应后,我们可以通过监测这些药物来测试cfr恢复药物。由于小管对Forskolin表现出类似的反应,并且可以从尿液中提取,因此它们可以作为一种侵入性较小的模型,以患者特定的方式测试cfr恢复药物。”
符合文森特的“3法则”,有一个强相关cftr恢复药物恢复肿胀反应与个体患者临床反应之间的差异。Geurts指出,当患者开始服用实验室鉴定的潜在有益药物时,该小组对其基于细胞的表型筛选试验的翻译相关性获得了信心:
“在我们实验室进行的基于细胞的表型药物筛选分析中,建立信心的最佳方法是直接在患者身上使用可能相关的药物。我们从一个有不同基因突变的病人身上提取了类器官雌性生殖道福斯克林诱导肿胀实验表明,Orkambi ® (lumacaftor/ivacaftor)导致类器官肿胀,表明患者有有益的反应。在该患者开始服用lumacaftor/ivacaftor后,他的症状明显减轻,表明我们的在体外表型药物筛选可以直接转化为患者。”
用形态分析把网撒得更宽
对于期望的表型未知的疾病,一些人认为基于图像的高含量筛查将提供价值和数百万美元合作都是为了证明这一点。传统的筛选分析侧重于量化少量预先选择的特征,与之相反,形态“分析”铸造一个更广泛的网络,以收集基于细胞形态的见解-一个潜在的丰富的数据源。由于担心使用单一的、人口平均读数的检测结果可能会产生低质量的结果,因此越来越多的检测结果出现努力在单个细胞水平上提取多个参数并改进图像处理,这在传统上是一项极其耗时的工作。现在,显微镜和图像分析可以自动化,实现高含量筛选和较少偏见的分析方法。
的细胞绘画该试验是由英国的研究人员共同开发的卡彭特和以下两麻省理工学院和哈佛大学布罗德研究所的实验室可以从每个染色和成像的细胞中产生大约1500个形态特征。测量的特征被整合到形态学轮廓中,包括染色强度、纹理模式、大小和八个标记细胞器的形状,以及跨通道的染色之间的相关性,细胞之间和细胞内结构之间的邻接关系(图1)。虽然大多数已发表的分析方法仅使用三种染料,但细胞绘画试验使用五种通道成像的六种荧光染色。
Cimini是联合领导开发的CellProfiler ™ 他指出,“表型分析的最大优势在于能够廉价、轻松地完成这项工作,然后能够建立关联。”这些关联可以用来选择从更有针对性的筛选方法中受益的化合物。在这一点上,西米尼强调了研究其中来自单一高通量成像分析的数据被重新用于预测其他(更昂贵或低通量)分析中化合物的生物活性,将命中率提高了50至250倍。
我们正在见证一个转折点吗?
作为总结最近遗传学家艾德里安·伯德爵士认为,“生物学已经成为一幅巨大的画布”——表现型筛查也不例外。表型筛选工具继续扩展,从微生理系统和形态分析,到基因编辑技术重现疾病状态在体外,基于图像的机器学习模型根据嵌入在图像中的表型特征预测化合物活性。希望我们将这段时间视为一个转折点,在药物筛选过程中提取更多生物学相关信息的努力将转化为临床成功率的提高。
广告


