如何加快药物开发的放弃某些临床试验

COVID-19大流行造成了全世界无数障碍临床研究。普遍的运动限制,医疗人员的分流前线和破坏能力,以确保参与者的安全的例子制药业面临的许多挑战。对临床试验的影响可能是长期的,创建一个迫切需要创新的策略,以确保未来的治疗发展的进展。
但是当今医药行业如何取得进展,仍得到产品市场面对这样的长期破坏?有可能在某些情况下消除人体试验的必要性?
高质量的在体外数据可以加快药物开发
药物开发过程的关键部分是建立药物吸收的速度和程度,这是一个复合的安全的关键因素。副作用可能发生如果药物释放到循环过快,虽然缓慢或不充分释放可能不足以产生预期的效果。 药物吸收通常是评估在人类研究通过测量 生物利用度,这是由美国食品和药物管理局(FDA)在21 CFR 320.1 “速度和程度的活性成分或活跃的一部分被吸收药物产品和网站的可用药物行动。”
而 动物实验可以用来定性分类药物 为低收入和high-bioavailability类,需要临床试验来确定最佳剂量浓度和方案。 临床研究正在挑战 在正常情况下;他们是费时,昂贵的和可以繁重的科目。在当前的环境下,我们正在见证临床试验管理员必须独特的导航 由于当前COVID-19流行所带来的各种问题 和理解,任何机会绕过人类研究代表了巨大的时间和成本节约;我们估计更换在活的有机体内生物利用度和生物等效性研究可以节省50 - 150美元的药物产品。
相比其他路线的政府绕过肠道吸收(如静脉注射,肌肉注射,皮下),口头管理产品的吸收更为复杂。 例如, 初步的消除 (在肝脏代谢或胃肠道)可以显著促进生物利用度可变性和 影响食物的摄入量 。因此,循环药物浓度必须测量评估系统性吸收和代谢的程度。在人体生物利用度研究中,两个重要的药代动力学参数测量:AUC(曲线下的面积-药物暴露和清除率的指标)和C马克斯(血清浓度峰值)。AUC和C马克斯也被用来证明生物等效性,根据需要在开发新的仿制药或不同的配方。
幸运的是,在口服药物管理的情况下,有很大机会快速发展的某些化合物类。通过收集从专业的高质量的数据在体外实验中,可以获得一个“biowaiver”作为人类的代理生物利用度和生物等效性研究。生物药剂学分类系统(BCS)是专为这个目的,使鉴定的化合物,符合标准BCS-based biowaiver。这个系统是通过药物分类的基础上的三个决定因素为速释固体口服剂型药物的吸收:
- 解散:化合物溶解的速度形成一个解决方案
- 水溶解性:溶质的最大浓度,可以溶解在一个给定的温度
- 肠道通透性:药物在胃肠道吸收的程度
BCS可以帮助药物开发者寻求创新的解决方案来帮助他们进步时药物开发在当前行业的挑战。
Biowaivers带来更多的好处比
通过利用biowaivers,开发人员将能够更好地抵御破坏看起来与我们保持在可预见的未来。限制不必要的涉及人体受试者的研究不仅有利于药物开发人员和监管机构通过时间和成本节约;缩短开发时间最终造福患者。取代人类的生物等效性研究在活的有机体内实验可以使药物可用,否则他们就会受阻或延迟由当前障碍临床试验,提供患者更早得到新的疗法。
在体外 生物利用度研究也喜欢某些化合物携带试验参与者的风险更高,比如那些上瘾的特性。从严格的收集数据在体外实验也可以带来更好的在以后的临床试验成功。例如,变量和高度复杂的药物活性药物成分(api)更容易在活的有机体内生物等效性故障,因此收购健壮在体外数据帮助容纳药物行为的可变性。
会发生什么:阶段BCS-based biowaiver应用程序
的 FDA-specified biowaiver资格的标准 是基于观察相关药物溶解,溶解和吸收。药物溶解的差异会导致药物吸收的速度和程度在医药上等价的固体口服产品明显不同。与快速溶解固体口服药物和高溶解度,药物吸收不太可能依赖于药物溶解在活的有机体内或胃肠道中转时间。提供使用的无活性成分的剂型不明显影响api的吸收,生物利用度或生物等效性在人类研究的示范可能,因此,没有必要。
获得biowaiver,药物化合物的问题必须被评估,分为以下BCS类:
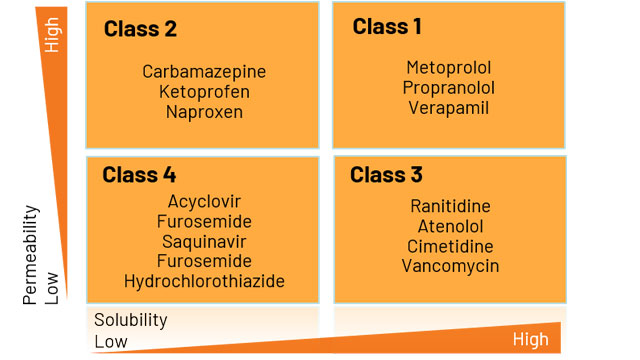
图1:图基于渗透性和溶解度BCS分类类别。
化合物分为类1和3是BCS biowaivers资格。美国食品药品监督管理局发布了细节BCS分类推荐测试方法,以及具体的参数,可用于定义是否药物高度可溶物质,高渗透,或迅速溶解。
biowaiver应用程序的过程可以分为四个主要阶段:
1)一个资格预审的步骤来确定资格
我们建议使用选定的,早期的实验提供一个决策点“行或不行”,确保下一阶段的化合物通过那些高满足FDA标准的机会。在这个阶段,主要有两个问题需要解决:
- 渗透率大于我们内部的标准吗?
- 射流比< 2 ?
正确的专业知识、资格预审的步骤可以采取1 - 2周,是一个机会来获得洞察药物的性质的物质,在分类。资格预审的步骤还用于建立药物物质系统的适用性问题,使用体外渗透测试只是推荐药物运输通过被动机制(即那些流出比< 2)。
2)优化协议FDA-mandated实验
协议进行了优化,以确保可再生的渗透率数据可以获得良好的实验室实践条件下,使用最具成本效益的选择。
3)BCS分类
FDA-mandated实验进行获得渗透率,溶解度和溶解数据使用下面讨论的方法。
4)应对FDA的提问
BCS biowaiver应用程序的最后阶段包括响应查询来自美国食品和药物管理局,以确保他们提供的数据感到满意。
生物药剂学分类的工具和方法
一个成功的BCS研究设计考虑哪些生理过程建模,包括适当的内部标准的使用。为在体外特别是渗透率测试、内部标准可以扮演了一个重要的角色在决定biowaiver的成功应用。高导磁率的内部标准(hpi)渗透率设置较低的阈值(P应用程序)在体外测试中,针对居民感兴趣的化合物进行比较。列为高度渗透性,渗透率的药物化合物必须不少于hpi的。
然而,最常用的HPISs有相对较高的P应用程序在Caco-2细胞单层(人类结肠癌细胞腺癌,使用最广泛的方法来评估肠道通透性),当预测增加II型错误的风险在活的有机体内渗透率。一个最优的hpi,较低P应用程序,建议在体外渗透率的研究。
增加鲁棒性和吞吐量, 多路复用系统允许多个剂量形式和/或多个参数进行评估 。小说也被开发系统,使溶解的药物产品的同步测量和吸收的API Caco-2细胞单层膜 ,这被认为是黄金标准在体外肠道通透性的预测。溶解度是单独评估,通常使用 标准shake-flask系统 。
一个战略方法促进biowaiver应用程序成功
在具有挑战性的环境下当前COVID-19大流行,需要创新方法来最大化促进药物开发的机会。幸运的是,通过一个独特的分类系统,可以获得豁免从人体生物利用度和生物等效性研究对于某些药物类。这使得药物开发公司前进,同时减少人类研究的必要性。因此,患者可以获得药物,否则可能无法进展。
BCS是由FDA提供战略,科学小说的分类框架和泛型化合物,根据他们的溶解度,解散和渗透率特征。这个系统使开发时间缩短为化合物分为类1(高溶解性、高磁导率)和3班(高溶解性、低渗透率),和重大努力针对改善biowaiver成功的机会。应用程序也可以受益于包含战略初步筛选步骤,行之有效的方法和最优的内部磁导率标准,从有经验的biowaiver应用程序专家和指导。
写的 克里斯•波德博士 。副总裁科学和企业沟通在吸收系统。

