新闻稿
英语
英语(pdf)
瑞典
瑞典(pdf)

新闻稿
2018-10-01
今天决定授予了吗
2018年诺贝尔生理学或医学奖
共同来
詹姆斯·p·埃里森和Tasuku Honjo
他们发现癌症治疗的抑制消极的免疫调节
总结
每年数以百万计的人死于癌症,是人类最大的健康挑战之一。通过刺激的固有能力我们的免疫系统攻击肿瘤细胞今年的诺贝尔奖获得者已经建立了一个全新的癌症治疗的原则。
詹姆斯p Allison研究已知蛋白抑制免疫系统的功能。他意识到潜在的释放刹车,从而释放我们的免疫细胞攻击肿瘤。然后他这个概念发展成一个品牌新方法治疗的病人。
同时,Tasuku Honjo发现一种蛋白质的免疫细胞,经过仔细的探索它的功能,最终显示,它也作为一个刹车,但具有不同的作用机制。疗法基于他的发现证明是非常有效的对抗癌症。
艾莉森和Honjo展示了不同的策略来抑制免疫系统的刹车可用于癌症的治疗。由两个奖构成的发现具有里程碑意义的对抗癌症。
我们的免疫防御可以从事癌症治疗吗?
癌症包括许多不同的疾病,特征是不受控制的异常细胞扩散和传播健康的器官和组织的能力。许多治疗方法可用于癌症治疗,包括手术、辐射、和其他策略,其中一些之前被授予诺贝尔奖。这些包括激素治疗前列腺癌的方法(哈金斯,1966),化疗(Elion和环节1988),为白血病骨髓移植(托马斯。1990)。然而,晚期癌症仍然是非常难以治疗,和新颖的治疗策略是迫切需要的。
在19世纪末和20世纪初的概念,激活免疫系统攻击肿瘤细胞可能是一个策略。试图与细菌感染患者激活防御。这些努力只有适度的影响,但是这种策略的一个变体是今天用于膀胱癌的治疗。这是需要意识到更多的知识。许多科学家从事激烈的基础研究和发现基本机制调节免疫力和还显示免疫系统如何识别癌细胞。尽管重大的科学进步,试图与癌症的发展可概括的新策略被证明是困难的。
加速器在我们的免疫系统和刹车
我们的免疫系统的基本属性是区分“自我”的能力从“异己分子”入侵的细菌,病毒和其他危险可以攻击和消除。T细胞(一种白细胞,这种防御的关键球员。表明T细胞受体结合自体和非这样的交互结构被认为是触发免疫系统的参与防守。但额外的蛋白质作为t细胞加速器也需要引发全面的免疫反应(见图)。许多科学家导致这一重要基础研究和确定其他蛋白质功能刹车T细胞,抑制免疫激活。这错综复杂的加速器和刹车之间的平衡对严格控制至关重要。它确保免疫系统充分参与攻击外国微生物,同时避免过度激活可导致自身免疫性破坏健康的细胞和组织。
免疫治疗的新原则
在1990年代,在他的实验室在加州大学,伯克利分校詹姆斯p Allison CTLA-4研究t细胞蛋白质。他是一些科学家观察的CTLA-4抑制T细胞功能。其他的研究团队利用机制作为目标治疗自身免疫性疾病。艾莉森,然而,有一个完全不同的概念。他已经开发了一种抗体,可以绑定到CTLA-4并阻止其功能(见图)。现在他着手调查如果CTLA-4封锁解除t细胞制动和释放免疫系统攻击癌细胞。艾莉森和同事在1994年底进行第一次实验,和兴奋立即重复圣诞假期。结果是出人意料的。老鼠已经治愈的癌症治疗的抗体抑制制动和释放抗肿瘤t细胞活动。尽管制药行业的兴趣,Allison持续强烈的努力发展战略为一个治疗人类。 Promising results soon emerged from several groups, and in 2010 an important clinical study showed striking effects in patients with advanced melanoma, a type of skin cancer. In several patients signs of remaining cancer disappeared. Such remarkable results had never been seen before in this patient group.
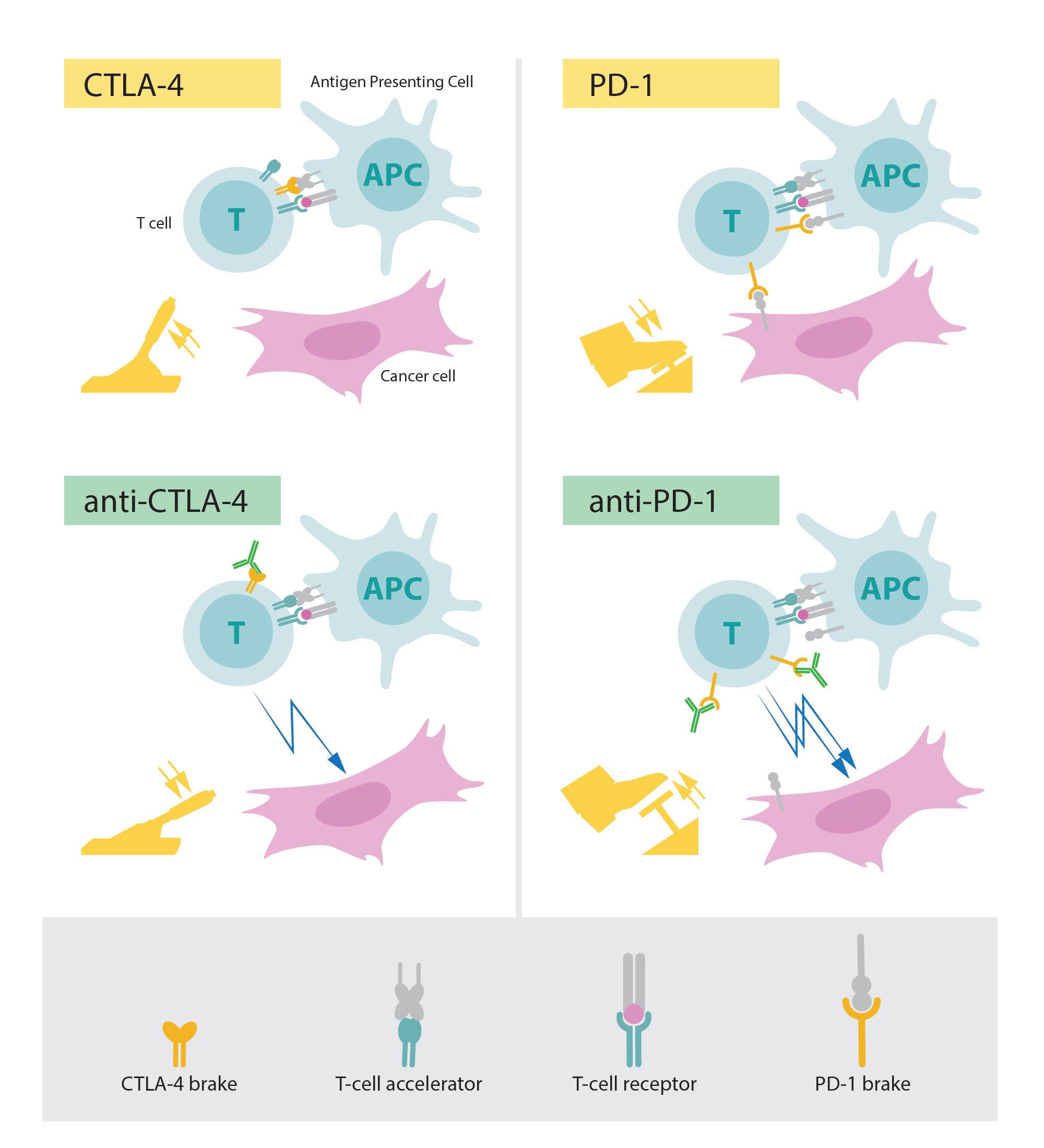
图:左上角:激活的T细胞需要T细胞受体结合结构在其他免疫细胞被认为是“异己分子”。蛋白质功能的T细胞加速器也需要T细胞活化。CTLA - 4功能抑制T细胞,抑制了加速器的功能。左下:抗体(绿色)对CTLA-4块制动的功能导致激活T细胞和攻击癌细胞。右上角:PD-1是另一种可抑制t细胞活化的t细胞刹车。右下:抗体PD-1抑制制动导致的功能激活T细胞和高效的攻击癌细胞。
发现PD-1和癌症治疗的重要性
几年前1992年,埃里森的发现,Tasuku Honjo PD-1发现,另一个t细胞表面的蛋白表达。决心解开它的角色,他小心翼翼地探索其功能在一系列的优雅实验执行京都大学多年来在他的实验室。结果表明,PD-1,类似于CTLA-4,函数作为t细胞刹车,但运营由不同机制(见图)。在动物实验中,PD-1封锁也被证明是一种很有前途的战略对抗癌症,Honjo和其他组织做了演示。这为利用PD-1铺平了道路作为目标治疗病人。临床开发后,在2012年的一个关键研究表明清楚功效治疗不同类型的癌症患者。结果是戏剧性的,可能导致长期的缓解和治疗转移性癌症患者在几个,以前认为本质上无法治愈的一个条件。
免疫治疗癌症检查站今天和未来
初步研究后显示的影响CTLA-4 PD-1封锁,临床急剧发展。我们现在知道,治疗,通常被称为“免疫检查点疗法”,从根本上改变了某些群体的晚期癌症患者的结果。类似于其他癌症治疗,副作用被认为,严重的甚至威胁生命。它们引起的免疫反应的过度导致自体免疫反应,但通常是可控的。强烈的持续研究侧重于阐明机制的行动,目的是提高治疗和减少副作用。
两治疗策略,检查点疗法对PD-1被证明是更有效和积极的结果中观察到的几种类型的癌症,包括肺癌、肾癌、淋巴瘤、黑色素瘤。新的临床研究表明,联合治疗,针对CTLA-4和PD-1可以更有效,在黑素瘤患者。因此,埃里森和Honjo鼓舞了努力结合不同的策略在免疫系统释放刹车,目的是消除肿瘤细胞更有效。大量的检查点疗法试验目前正在进行对大多数类型的癌症,和新的检查点蛋白质被测试为目标。
100多年来,科学家们试图让免疫系统对抗癌症。直到两奖获得者,重要发现的进展为临床开发是适度的。检查点已经变革了癌症治疗和治疗已经从根本上改变了我们认为癌症是如何管理的。
主要出版物
石田,Y。,Agata, Y., Shibahara, K., & Honjo, T. (1992). Induced expression of PD-1, a novel member of the immunoglobulin gene superfamily, upon programmed cell death.EMBO J。,11(11),3887 - 3895。
Leach, d R。,Krummel, M. F., & Allison, J. P. (1996). Enhancement of antitumor immunity by CTLA-4 blockade.科学,271年(5256),1734 - 1736。
Kwon e D。,Hurwitz, A. A., Foster, B. A., Madias, C., Feldhaus, A. L., Greenberg, N. M., Burg, M.B. & Allison, J.P. (1997). Manipulation of T cell costimulatory and inhibitory signals for immunotherapy of prostate cancer.《美国国家科学院刊,94年(15),8099 - 8103。
Nishimura H。、鼻子、M。Hiai, H。,Minato, N., & Honjo, T. (1999). Development of Lupus-like Autoimmune Diseases by Disruption of the PD-1 gene encoding an ITIM motif-carrying immunoreceptor.免疫力,11,141 - 151。
弗里曼G.J.长,抗干扰自制,Y。,Bourque, K., Chernova, T., Nishimura, H., Fitz, L.J., Malenkovich, N., Okazaki, T., Byrne, M.C., Horton, H.F., Fouser, L., Carter, L., Ling, V., Bowman, M.R., Carreno, B.M., Collins, M., Wood, C.R. & Honjo, T. (2000). Engagement of the PD-1 immunoinhibitory receptor by a novel B7 family member leads to negative regulation of lymphocyte activation.J Exp地中海,192年(7),1027 - 1034。
Hodi, F.S.,Mihm, M.C., Soiffer, R.J., Haluska, F.G., Butler, M., Seiden, M.V., Davis, T., Henry-Spires, R., MacRae, S., Willman, A., Padera, R., Jaklitsch, M.T., Shankar, S., Chen, T.C., Korman, A., Allison, J.P. & Dranoff, G. (2003). Biologic activity of cytotoxic T lymphocyte-associated antigen 4 antibody blockade in previously vaccinated metastatic melanoma and ovarian carcinoma patients.《美国国家科学院刊,One hundred.(8),4712 - 4717。
自制,Y。,Terawaki, S., & Honjo, T. (2005). PD-1 blockade inhibits hematogenous spread of poorly immunogenic tumor cells by enhanced recruitment of effector T cells.Int Immunol,17(2),133 - 144。
詹姆斯·p·埃里森生于1948年的爱丽丝,德克萨斯州,美国。他在1973年获得博士学位德克萨斯大学,奥斯丁。从1974年到1977年他是一个博士后研究员斯克里普斯诊所和研究基金会,加州拉霍亚。从1977年到1984年他在德克萨斯大学教员系统癌症中心,Smithville德州;从1985年到2004年在加州大学伯克利分校和从2004年- 2012年纪念斯隆-凯特林癌症中心,纽约。从1997年到2012年他是一个霍华德休斯医学研究所研究员。自2012年起,他一直担任教授的德克萨斯大学MD安德森癌症中心,休斯顿,德克萨斯州和附属于帕克癌症免疫疗法。
Tasuku Honjo1942年出生于日本京都。1966年,他成为了医学,从1971 - 1974年他在美国华盛顿卡内基研究所的研究员,巴尔的摩国立卫生研究院,马里兰州贝塞斯达。他在京都大学在1975年获得博士学位。从1974年到1979年他是一个教员在东京大学和大阪大学从1979年到1984年。自1984年以来,他一直在京都大学教授。他是一个教师院长从1996 - 2000和2002 - 2004年在京都大学。
插图:©诺贝尔生理学或医学奖委员会。插画家:这张Karlen
诺贝尔大会,由50个卡罗林斯卡医学院教授,奖项诺贝尔生理学或医学奖。诺贝尔委员会评估提名。自1901年以来,诺贝尔奖被授予的科学家做出了最重要的发现,造福人类。
诺贝尔奖®是诺贝尔基金会的注册商标
诺贝尔奖,获奖者
看到这里介绍。

