新晶体结构(Ph) PINK1艾滋病对早发性帕金森病的认识
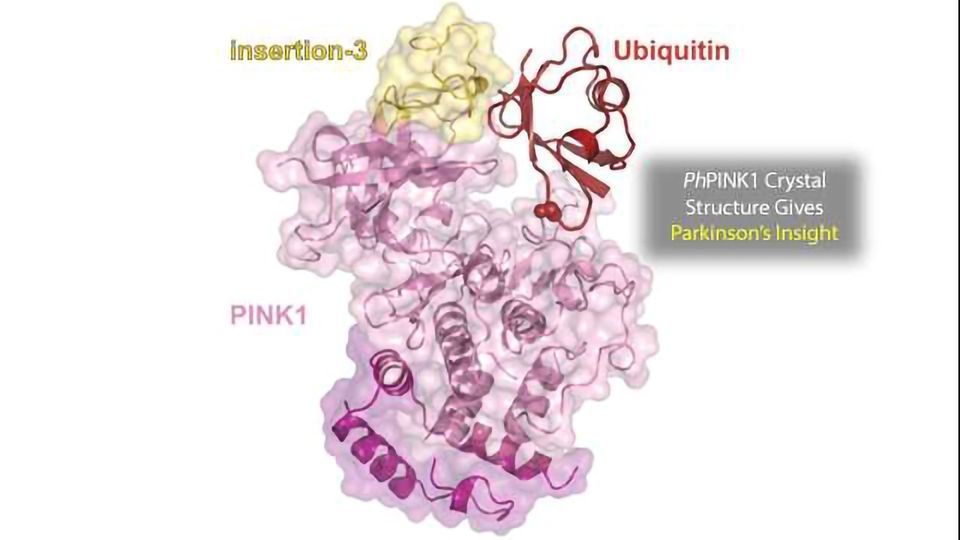
神经退行性疾病的帕金森症通常是发现在60岁以上,但是大约10%的情况下常染色体隐性的少年形式在一个公园的基因突变,造成15已标注日期。PINK1编码产生一个对丝氨酸/苏氨酸激酶,是第一个公园基因被识别,也是最不同的蛋白激酶。PINK1触发间隙通过磷酸化的小监管受损的线粒体蛋白质的泛素。最近,一个新的构象的泛素被发现,被称为泛素c端收回了构象,或Ub-CR。这个新泛素构象可以稳定点突变(乌兰巴托TVLN),它可以表明,结合PINK1比野生型高亲和力的形式。此外,似乎Ub-CR构象PINK1需要高效的磷酸化。
尽管其散度与其他人类的蛋白激酶,PINK1之间高度保守的物种导致识别昆虫同系物,(Ph) PINK1,可以更容易地表达在实验室进行实验。在最近的一项研究,科学家们就能够确定PhPINK1绑定到乌兰巴托的晶体结构的帮助下TVLN nanobody稳定作用。亚历山大·舒伯特博士研究的第一作者,评论道“虽然PINK1一直得到广泛的研究在过去的十年,是不可能使具体化这高度动态的蛋白质。因此我们没有理解这种不同寻常的激酶如何运作,如何能够使磷酸化泛素。泛素,另一方面,也是一个非常不寻常的激酶衬底,其磷酸化网站(Ser65)并不容易。PINK1高度突变在早发性帕金森症和结构我们可以理解几个病人突变在分子水平和可能引导帕金森病治疗的设计”。
复杂结构有助于理解40多个PINK1基因突变的分子基础,这可能会导致有害的变化,导致帕金森病。希望这些信息会使帕金森病治疗的设计。Alex得出结论“在其活性构象PINK1结构绑定到其衬底泛素是一个很好的起点PINK1-activating小分子的发展。我们都很积极,我们的结构将指导药物来治疗的设计在未来早发性帕金森病。“在更广泛的背景下,结构也揭示了信息如何激酶酶家族,这是一个主要的药物目标本身,与基质开门的改善许多退行性疾病的治疗。
参考
PiNK1结构在复杂的基质泛素亚历山大·f·舒伯特Christina Gladkova Els)对不起,简·l·瓦格斯塔夫,Stefan号Freund, Jan Steyaert莎拉·l·套装和大卫Komander。自然http://dx.doi.org/10.1038/nature24645 (2017)。


