加快肝脏基因药物发展

最近的技术进步已经有机会提高基因和细胞药物的效率、功效和安全性,以治疗多种遗传疾病。迄今为止,该领域面临的主要挑战是能够将治疗性基因传递到受影响的细胞类型。然而,最近临床基因治疗试验的结果提供了证据,至少对于某些疾病,这一挑战已经被克服。例如,腺相关病毒(AAV)载体已被用于成功地将治疗基因传递到肝脏、视网膜和大脑。此外,慢病毒载体已被成功用于体外造血干细胞的治疗基因,这些修饰细胞已被用于治疗免疫,血液和神经疾病,一个主要的例子是CAR-T治疗癌症。从这里开始,随着产品开发人员转向下一代表达结构,紧密、靶向和稳健的基因调控和新型启动子元件的重要性已经出现。
肝是基因转移治疗的理想靶点各种遗传代谢和获得性疾病.除了急性和慢性肝衰竭外,肝移植还可以纠正各种先天性代谢错误,例如:
•家族性淀粉样变性
•遗传oxalosis
•α1‐抗胰蛋白酶(AAT)缺乏
•威尔逊氏病
•酪氨酸血症,I型和IV型糖原储存疾病
•Niemann优先选择疾病
•Crigler‐Najjar综合征1型(CN1),尿素循环酶缺乏症
•C蛋白缺乏症
•血友病A和B2
重组病毒用于肝脏基因转移的适用性是基于有几个因素包括可达到的感染效价、病毒感染非分裂细胞的能力、融入宿主基因组的效率、给药的可重复性、对病毒和转基因的有限免疫反应以及载体系统的安全性。目前有4大障碍成功的病毒基因治疗。这些过程包括(1)病毒的摄取、运输和脱壳;(2)载体基因组持久性;(3)转录持久性;(4)免疫反应。
肝脏基因治疗-超越载体取向
人肝细胞的高效转导是aav介导的基因疗法成功应用于肝病治疗的关键。优化转录控制元件可以改善肝脏中的转基因表达.一个AAV产品可以被设计成限制转基因的表达,按照不同的全身给药途径,但添加组织特异性启动子来选择性地驱动转基因的表达,显著提高了载体的安全性,因为它将(a)从抗原呈递细胞中去靶向表达,从而抑制免疫反应;(b)限制在非靶细胞中的表达,从而减少潜在的破坏性脱靶副作用的机会。
提高转录控制-新的合成启动子设计基因药物产品规格
Synpromics已经开发了一个技术平台PROMPT®和一个专有的机器学习方法来创建启动子候选库,这些启动子候选库是根据一套谨慎的规范设计和开发的。这些规格可以包括启动子的大小,启动子的组织、细胞或多细胞类型的选择性,以及启动子的强度。规格还可以包括启动子是否在靶细胞类型中构成性表达或在细胞中被调节或诱导。这些启动子既可用于体内基因医学(替代疗法或基因组编辑),也可用于体外基因修饰细胞治疗应用。需要新的启动子来驱动高效的、精细调节的基因表达,从而使治疗效果安全、定向和持久,超过了载体衣壳所能提供的效果。此外,考虑到目标基因可以使用免疫原性载体(病毒和细胞)传递,而且治疗基因通常是新的,需要尽量减少对治疗盒的长期免疫反应。
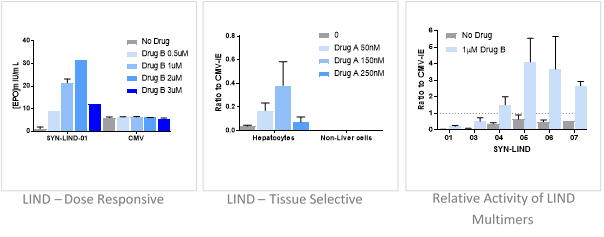
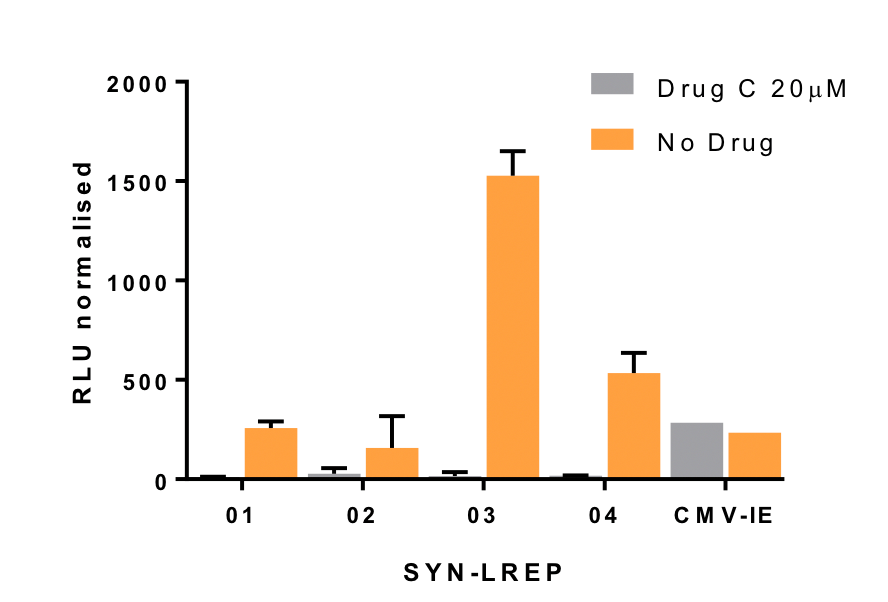
为了解决这些问题,Synpromics已经建立了其合成启动子平台,以满足基因药物产品开发者的谨慎需求。下面的三幅图是设计用于改善肝脏定向基因药物的新型启动子系统的例子。强度和大小用于增加效力(图1),通过口服控制和药物反应诱导系统(图2)和抑制系统(图3)实现严格的基因调控。这些潜在的改善安全性和有效性启用否则不可寻址的基因药物靶标。

上下文是关键:表达式盒的优化
对所有基因药物的持续发展至关重要的是对基因产物表达盒中调控元件的最佳环境的深刻理解。这包括关注末端重复序列在基于病毒的结构中的作用,因为需要设计表达盒来优化倒置末端重复序列(ITRs)与启动子和调控元件之间的关系,因为错误放置可以以积极和消极的方式影响启动子活性。此外,智能基因药物设计专注于内含子在表达盒中的作用。内含子控制着mRNA的加工,因此是一个关键的转录后通路,当被设计成一个表达盒时,可以在体内进行更有效的翻译。内含子还可以通过转录后控制机制进一步调节蛋白质表达水平。最后,由于5 ' /3 ' utr赋予了mRNA的稳定性,它们也应该被纳入设计中,识别能够进一步影响蛋白质表达的utr很重要。Synpromics的卡带设计考虑到了所有这些元素。
总结
目前有了优化的衣壳,基因药物产品开发人员现在专注于利用新技术和合成启动子系统来更准确地靶向和微调包括肝脏在内的多种组织的组织表达。在Synpromics,我们正在开发创新的合成启动子和新的调控系统,以满足基因治疗部门对更严格和更准确的转录控制的需求。这些改进将促进当前产品的开发,重要的是使未来的改进能够解决更复杂的肝脏疾病。




