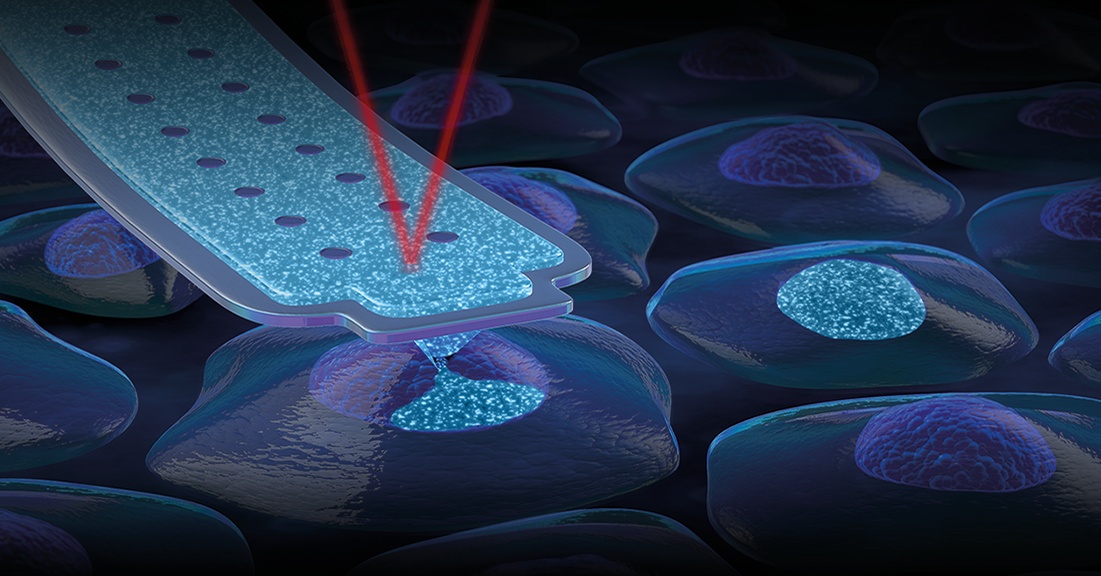
奥林巴斯感到骄傲与Cytosurge合作成为一个完整的系统提供商科学界不断增长的需要下一代单细胞和CRISPR基因操作的解决方案。
的需求持续上升,同时研究人员看到他们的潜力研究疾病,寻找医学治疗,,造福人类健康。Cytosurge FluidFM遗传操作提供了一个强大的解决方案®全部(以前称为FluidFM机器人生物系列),一个高度自动化系统建立在奥林巴斯IX83倒置显微镜与奥林巴斯的著名光学。除了CRISPR基因组编辑,系统允许前所未有的研究在广泛的应用。在神经科学,例如,研究人员可以生成图案的神经网络,在单细胞组学,他们可以执行重复的抽取,同一细胞的胞质。
FluidFM模式各种各样的应用程序
不同的尖端形状、孔径大小和机械规格FluidFM探针支持三个基本modes-pick和地点,注入和抽样,和本地化dispensing-enabling创新应用神经科学、病毒学、力学生物学或CRISPR细胞系的发展。

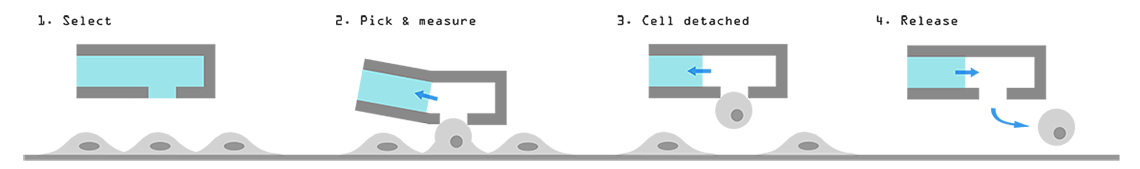
选择和地点
抓住和迁移单个细胞
其他实例对象。
注入和抽样
注入和提取从单个细胞可能量化注射或提取体积。

本地化的调剂
分配少量的液体,
在空气中或浸泡。
神经科学
FluidFM技术是一种新颖和创新的工具箱,开辟了一个数组操纵单一神经元的可能性。通过联合最优特性的微流体和力显微镜使用不同的控制力探针,FluidFM技术提供了一个广泛的创新方法,从单细胞操纵控制的增长,刺激,和分析,以温和的方式适合敏感的神经元细胞等。
- 模式
定义,轴突生长。 - 选择和地点
构建微脑通过创建神经网络。 - 刺激
应用神经递质神经元上的任何地方。 - 注入
交付CRISPR复合物直接进入细胞核。 - 观察
跟踪你的操纵神经元。 - 分析
提取神经元细胞内容同时保持完好无损,活着。
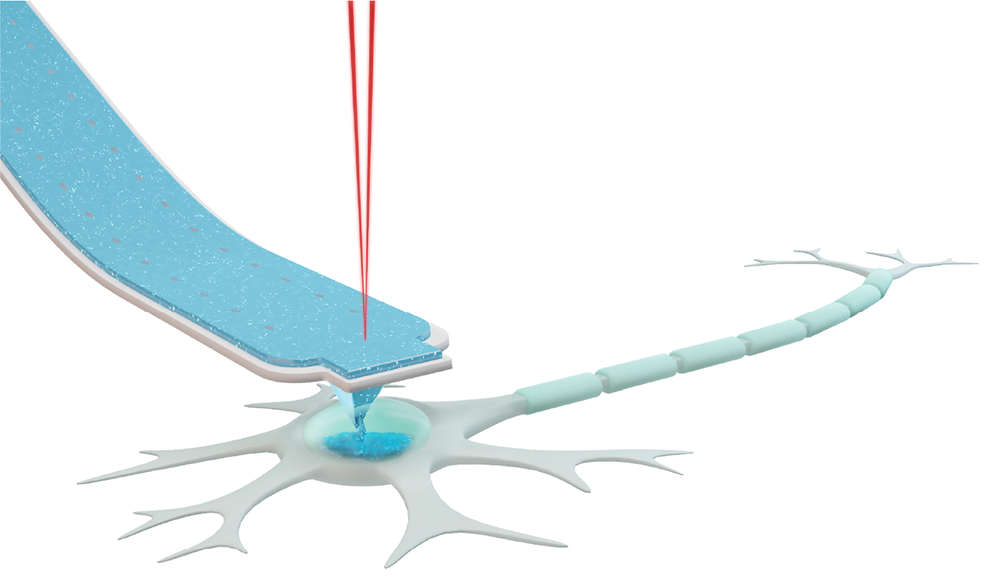
刺激,注入,观察单个神经元与FluidFM技术。由Cytosurge AG)。
病毒学
超越大部分experiments-study病毒入口和复制在一个virion-single细胞水平。温和,微通道,力回馈控制FluidFM探针,单一的病毒粒子可以放置在选定的细胞,使前所未有的控制来研究病毒感染体外。FluidFM技术可以帮助照亮毒性基本问题,病毒复制,或宿主的免疫反应,增加新的抗病毒药物和疫苗的发展。
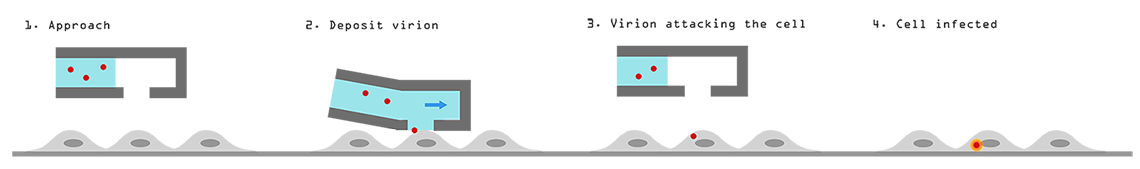
病毒与FluidFM操纵技术的工作原理。由Cytosurge AG)。
- 精确的存款一个病毒粒子
单一的病毒粒子可以被放置在一个精确的位置在你的细胞的选择。 - 注入一个病毒粒子
直接注入一个病毒粒子一个特定细胞的细胞质或细胞核。 - 测量生物物理变化
测量质量的变化、刚度的变化,和粘附力的变化。 - 分离、提取和分析
隔离受感染的细胞或单细胞的活组织检查或分析进一步扩张。 - 观察和监控
持续监测细胞,观察周围的文化通过显微镜和跟踪软件集成。
力学生物学
而传统的细胞需要粘在AFM悬臂,Cytosurge FluidFM技术可逆固定细胞通过吸入FluidFM调查,并随后释放压力脉冲或短暂的洗涤。这温柔的交换单元使悬臂长期被重用,节省时间和成本,并导致高吞吐量,增加你的生产率提高了10倍以上*光谱学方法相比传统的力量。测量机械数据高达每天200细胞由于与FluidFM可逆细胞固定化技术。
- 简单和可逆固定化
可逆的依恋的对象通过吸悬臂。 - 巨大的力量范围
测量从pNµN。 - 许多细胞类型和胶体
对哺乳动物细胞、微生物和胶体。
单细胞的工作原理与FluidFM光谱学技术力量。由Cytosurge AG)。
*每天1 - 3细胞相比光谱测量的典型传统的力量。
相关视频
Nanoprinting
FluidFM与其微流控技术探测提供了前所未有的多功能性和控制打印模式,探索纳米结构的创建。你是否正在与蛋白质阵列传感应用,化学梯度细胞迁移研究,想理解化学过程在飞升滴,或者有兴趣开发下一代纳米加工processes-FluidFM技术为你的研究打开了新的大门。
- 从飞升到只
只打印飞升水滴或存款。 - 从纳米到厘米
打印功能的300 nm和创建模式厘米范围内。 - 1到10 000 cP粘度
用户有印刷油墨从1到10 000 cP,从水到蜂蜜。 - 在空气和液体
FluidFM技术工作沉浸和环境条件。 - 广泛的油墨
水、缓冲、油、酸、溶剂、纳米粒子等。
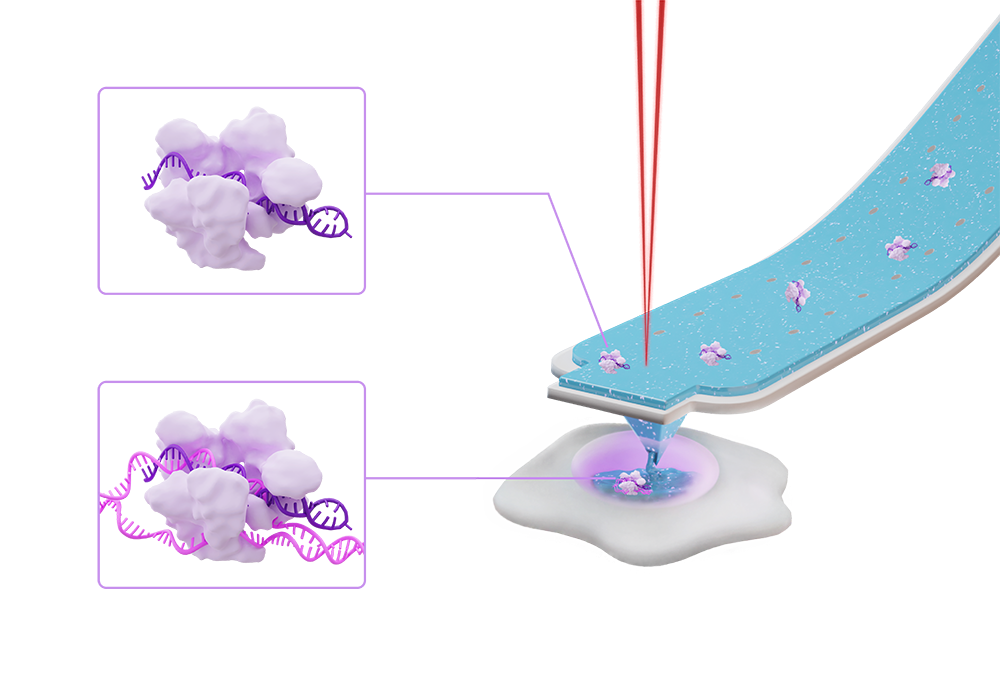
单个细胞组学
FluidFM技术无损,单细胞生活组学提供了一个有趣的解决方案。由于其温和的细胞操纵技术,FluidFM技术使subpicoliter卷的提取从一个细胞的细胞质或细胞核和分离提取的内容进行进一步分析。这个细胞质活检是如此温柔的细胞存活,和顺序活检可以完全相同的细胞。通过避免破坏性的细胞裂解,轨迹端点分析成为可能,无论是在转录组,代谢组学,蛋白质组学,或任何其他组学研究。
- 无损提取
轻轻地从细胞质或核同时保持细胞存活和完全可行的。 - 保存的生理环境
开采期间,保持上下文的目标细胞旁边周边细胞和节约建立信息交互。 - 时间进程活组织检查
温柔的提取重复了几次相同的细胞,例如,刺激的一个特定的药物。 - 选择和地点
如果需要完整的单元内容,隔离直接从一个附着或悬浮培养细胞而不影响邻近的细胞。
相关视频
提取细胞与FluidFM内容。由Cytosurge AG)
保持长期的关注
在长期的成像方法,保持焦点的位置是关键,环境温度变化引入的热漂移补偿必须准确。奥林巴斯的激光TruFocus™Z-drift补偿制度有助于确保样本总是焦点产生最大图像成为可能。近红外激光不断检查,如果需要调整焦点的位置,确保细胞仍集中在长期延时实验。
微秒级精度提高细胞生存能力
奥林巴斯实时控制器(RTC)功能独立的CPU板,提供快速、并行实验执行没有延迟,即使在复杂的实验装置。这导致计时精度高和精度小于2µs,这对高速成像是至关重要的。
精确的设备控制,良好的定时精度,高精度需要减少样本漂白,细胞生存能力最大化,并提供数据重复性和RTC交付所有三个。
在不同的应用程序的更多信息,请访问www.cytosurge.com/applications
引用
技术
- a·迈斯特·m·加比,p . Behr p、j .用途:p .涅,j . Bitterli j . Polesel-Maris m . Liley h . Heinzelmann Zambelli。FluidFM:结合原子力显微镜和纳米流体力学对单个细胞的普遍液体输送系统应用程序和超越。(2009)纳米快报,9 (6),2501 - 2507。
神经科学
- m . j . Aebersold h . Dermutz l . Demko j·f·萨恩斯Cogollo,研究所。林,c . Burchert m·施耐德d .凌c,跳弗乐韩h . t . Zambelli试图购买。当地的化学刺激神经元与射流力显微镜(FluidFM)。(2017年11月)ChemPhysChem, 1439 - 7641。doi: 10.1002 / cphc.201700780
- h . Dermutz水银血压计Gruter、点Truong l . Demko j .用途:Zambelli。当地原位聚合物替代神经元模式和神经突的指导。朗缪尔:美国癌症协会杂志》上的表面和胶体,30 (23),7037 - 46。doi: 10.1021 / la5012692
- o . Guillaume-Gentil随机变数Grindberg, r . Kooger l . Dorwling-Carter诉马丁内斯,d . Ossola m . Pilhofer t Zambelli J.A. Vorholt。可调单细胞提取分子分析。(2016年7月),166 (2),506 - 516。doi: 10.1016 / j.cell.2016.06.025
CRISPR细胞系发展
注射和隔离出版物:
- o . Guillaume-Gentil e . Potthoff et al。控制力射流注入单细胞核。小,2013。
- 崔y、x律l .叮,l·柯·d·杨,m . Pirouz y气,j . Ong g高,p . Du也是格雷戈里。全球microrna的剂量控制胚胎胚芽层规范。(2021)。doi.org/10.1038/s41586 - 021 - 03524 - 0
- Guillaume-Gentil, O。Zambelli, T。Vorholt, j . a (2014)。孤立的单一的哺乳动物细胞附着文化由射流力显微镜。芯片上的实验室,14 (2),402 - 414。https:// doi.org/10.1039/c3lc51174j
病毒学
- p•施蒂费尔F.I.施密特,p . Dorig, p . Behr t . Zambelli j . a . Vorholt和j·默瑟。合作使用FluidFM痘苗病毒感染在单细胞水平。纳米快报,2012年。
- 克勒,M。佩提特金,S.J.L.杨,J。Aravamudhan, P。Somoulay X。Lo Giudice C。Poncin,硕士Dumitru,交流,T.S. Alsteens Dermody D。呼肠孤病毒直接参与整合素招募网格蛋白进入宿主细胞。自然通讯(2021),2149。doi: 10.1038 / s41467 - 021 - 22380 - 0
力学生物学
- a . Garitano-Trojaola桑丘,r . Goetz s Walz h . Jetani e . Teufel n . Rodhes m . DaVia l . Haertle s Nerreter c·沃格特j·杜埃尔说r . tib,克劳斯,a·罗森沃尔德l . Rasche m . Hudecek m·萨奥尔h . Einsele格罗尔j . m . Kortum。RAC1抑制剂EHT1864 Venetoclax克服Midostaurin阻力在急性髓系白血病(aml)。(2019)的血液。- 2019 - 129762 . doi: 10.1182 /血
- n . Chala s Moimas c . Giampietro x张t . Zambelli诉Exarchos T.Z. Nazari-Shafti, d . a Poulikakos法拉利。机械的指纹在内皮细胞衰老。(2021)纳米快报。
- f·梅,郭y y黄马,y, x, m .徐y,邓公元前亨,陈l . x。通过p-PXN-Rac1-YAP信号矩阵刚度调节提示细胞形成轴。(2021)生物活性材料。
- l . Hofherr c . Muller-Renno齐格勒。FluidFM作为一种工具来研究细菌的粘附力,优化参数和比较传统的细菌探针扫描光谱。(2020)。PLOS ONE。doi: 10.1371 / journal.pone.0227395
- k .娃娃,i, e . Fadeeva n . Kommerein s . p . Szafranski g . b . der Wieden a . Greuling a·温克尔b . n . Chichkov n s Stumpp Stiesch。Liquid-infused结构化钛表面:Antiadhesive机制击退链球菌oralis生物膜。(2019)ACS达成。板牙。接口。doi: 10.1021 / acsami.9b06817
- m . Mittelviehfhaus D.B. cooper穆勒,t . Zambelli J.A. Vorholt。模块化的原子力显微镜的方法揭示了一个大范围的疏水性细菌之间的粘附力叶微生物群的成员。《ISME日报》(2019年)。doi: 10.1038 / s41396 - 019 - 0404 - 1
Nanoprinting
- b . j . Zhang h . Yu哈里斯,等。新方法来控制分子组装。ACS的出版物,2020年。
- 答:Saftics et al。仿生dextran-based水凝胶层细胞缩微成像在大面积使用FluidFM机器人技术。朗缪尔,2019
- j·w·s . Mishra y•李公园。直接量化慢性骨髓性白血病微量的生物标志物使用锁核酸捕获探针。分析化学,2018年。
- m . j . Aebersold et al。当地的化学刺激神经元与射流力显微镜。(FluidFM)。ChemPhysChem, 1439 - 7641, 2017。
- de Souza J.V. et al。三维Nanoprinting通过直接交付。物理化学学报B, 2017。
- h . Dermutz et al。当地原位聚合物替代神经元模式和神经突的指导。朗缪尔:美国癌症协会杂志》上的表面和胶体,30 (23),7037 - 2014。
单个细胞组学
- o . w . Chen Guillaume-Gentil, r . Dainese, p . Yde Rainer, m . Zachara c . g . Gabelein j . a . Vorholt Deplancke。全基因组分子使用Live-seq记录。(2021年3月)bioRxiv 2021.03.24.436752
- o . Guillaume-Gentil t·雷伊·基弗A.J. Ibanez说,r . Steinhoff r . Bronnimann l . Dorwling-Carter t . Zambelli r . Zenobi J.A. Vorholt。单细胞代谢物从生活中提取细胞的质谱分析射流力显微镜。(2017年5月)肛门化学。89 (9),5017 - 5023。doi: 10.1021 / acs.analchem.7b00367
- o . Guillaume-Gentil随机变数Grindberg, r . Kooger l . Dorwling-Carter诉马丁内斯,d . Ossola m . Pilhofer t Zambelli J.A. Vorholt。可调单细胞提取分子分析。(2016年7月),166 (2),506 - 516。doi: 10.1016 / j.cell.2016.06.025。
对不起,该页面
可以在你的国家。
对不起,该页面
可以在你的国家。