在基因组:表观遗传学如何影响癌症和肥胖

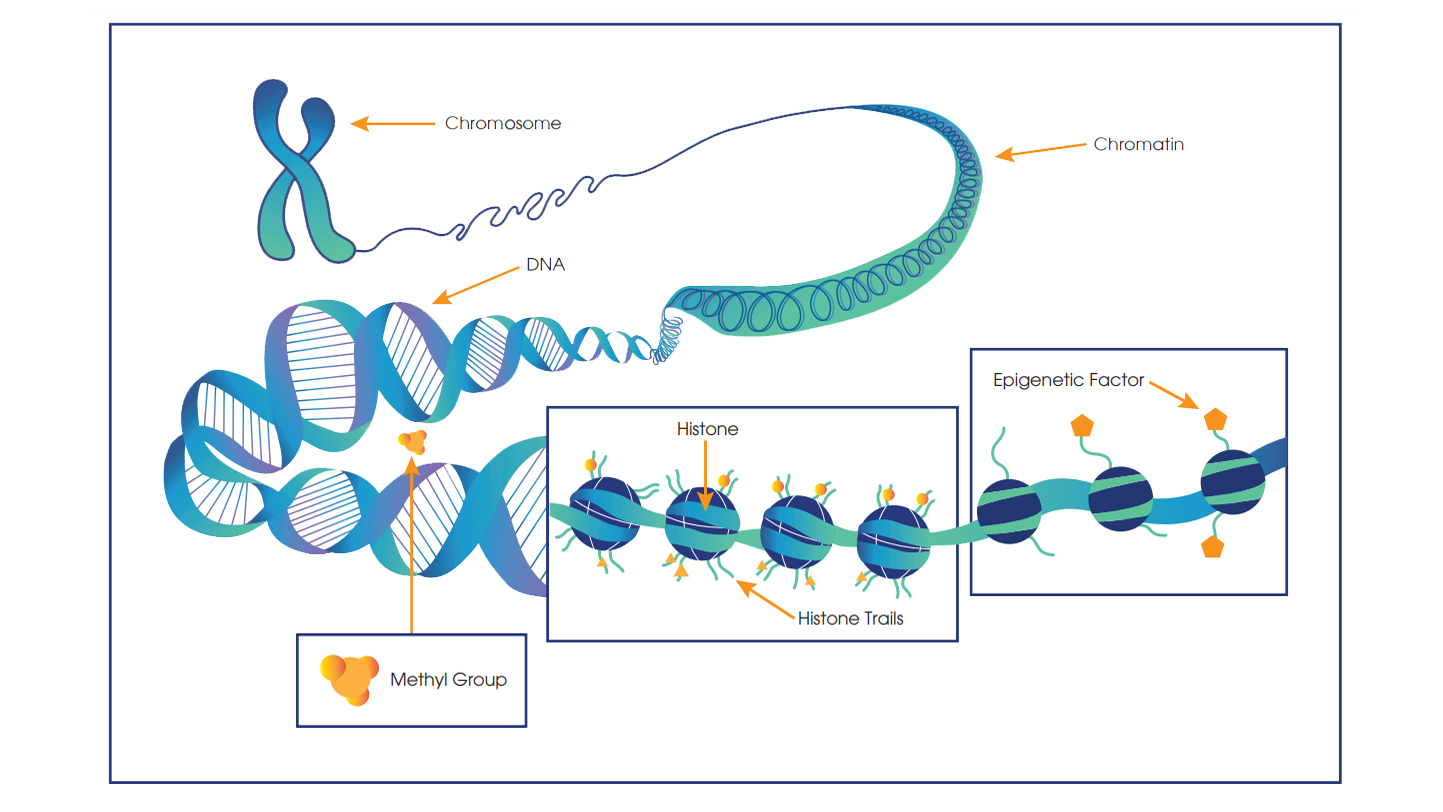
真正理解我们的DNA如何影响我们的生活和健康有时意味着过去的DNA序列。实验胚胎学包括一组遗传修改不改变DNA序列本身,这是遗传学领域。表观遗传学其根源来自希腊语前缀“epi”的意思是“上面”或者“结束了,”当与“遗传学”“表观遗传学”字面意义为“最重要的基因,”暗指一个额外的层除了遗传基因遗传特征。表观遗传变化可以通过多种机制来实现,如修改DNA碱基,例如,通过甲基化的胞核嘧啶,改变组蛋白蛋白质甲基化和乙酰化,例如,一位将军染色质的重塑最终导致的变化基因表达谱。
放松管制的表观基因组可以对我们的健康产生深远影响,因此表观遗传学在近几十年来越来越欣赏惊人数量的疾病。虽然癌症位列榜首,表观遗传学了肥胖,代谢综合征和糖尿病,老化,心血管疾病,肾脏和肝脏疾病,自身免疫,如类风湿性关节炎,过敏性疾病和炎症等疾病克罗恩氏病和炎症性肠病。表观遗传学中也扮演了重要的角色抑郁症,神经系统和神经退行性疾病包括阿尔茨海默病。
利用表观遗传癌症放松管制
异常的表观遗传学的核心功能是许多癌症和长期以来一直是密集的研究领域。表观遗传学可以改变扩散,细胞循环发展,新陈代谢,转移潜能癌症细胞,最终推动肿瘤发生和疾病进展。一些治疗癌症的药物针对后生管制获得FDA批准,等组蛋白脱乙酰酶抑制剂(iHDACs),烷基化,脱甲基代理,除了药物临床前和临床发展。
虽然已经取得了很大进展,尤其是血液癌症,表观遗传管制继续成为一个问题在一些癌症。最近,几种类型的脑肿瘤是epigenetically管制,如突变体异柠檬酸脱氢酶1/2 (mIDH1/2)低级神经胶质瘤和儿科高档扩散内在脑桥的神经胶质瘤(DIPG)。mIDH1/2神经胶质瘤DNA和组蛋白甲基化特征是由于改变了细胞的新陈代谢。methylome的重组,这是组蛋白与DNA碱基的模式修改整个基因组甲基化,最终认为驱动肿瘤发生和药物针对mIDH1/2酶临床开发。
DIPG癌症是一种致命的童年与一个特别贫穷的生存中值11个月。传统疗法只产生适度的改进在病人的结果,迫切需要新的治疗途径。DIPG肿瘤的分子分析最近发现了有史以来第一次组蛋白蛋白质突变组蛋白3 (H3),最常见的氨基酸K27 M (H3K27M)。博士回忆说“这是一个惊喜,“辛西娅·霍金斯,神经病理学家和高级科学家,儿童医院,多伦多。“虽然变更涉及PRC2复杂,特别是其EZH2域,先前描述的其他癌症,这是第一个报告一个组蛋白基因的突变。“PRC2或polycomb压制复杂2,组蛋白甲基化酶,即。甲基转移酶,参与调控的表观基因组。超表达或突变PRC2已经知道驱动几种类型的癌症。
理解驾驶表观遗传机制管制可以揭示潜在的治疗靶点和是一个密集的研究领域在突变H327M DIPG。H3K27M突变改变了K27残渣,一个经常被甲基化氨基酸。“变异H3K27M组蛋白被表示为一个很小的比例(~ 5 - 15%)的总H3因为有多个基因编码H3,不是因为野生型等位基因表达更强烈,”霍金斯博士解释说。然而,这一小部分的表达突变H3K27M驱动全球hypomethylation净。“这种影响的机制被认为发生抑制EZH2甲基转移酶PRC2领域。PRC2被认为获得锁突变蛋氨酸残渣,防止沿着混入甲基邻野生型的染色质组蛋白,在H3K27进行甲基化状态在整个基因组与一些地区出现trimethylation损失和其他收益。“总的来说,一个改变methylome有几个下游影响DIPG肿瘤。
这意味着一个潜在的治疗?“针对突变组蛋白直接被证明是困难的,”霍金斯博士的反应。“有一个开放的试验使用immunotherapy-based战略目标肿瘤细胞;但是,尚未有戏剧性的反应这一策略。其他试验针对更一般的表观遗传机制被认为是基于临床前数据等正在进行中HDAC抑制剂,EZH2抑制剂,BMI-1抑制剂”。
组学给肥胖
肥胖是一个多因子的疾病产品的环境因素如饮食摄入量和内在的等遗传素质。虽然早期的调查集中在饮食消费的主要原因,相对稳定的肥胖比瘦的人在相同的致胖环境建议变异和个体之间的倾向。识别这些因素已经被组学的崛起更容易系统范围的方法,革新了肥胖的研究。例如,全基因组关联研究(GWAS)已经确定了关键与遗传易感性与肥胖相关的位点。
然而,GWAS研究发现的位点不占所有观察到的遗传肥胖,导致调查潜在的肥胖的表观遗传贡献。早期的研究检查特定的,单个位点,但epigenome-wide协会研究(ewa)已经确定了更多的位点。“表观遗传修饰的影响,如DNA甲基化,对肥胖的发展已经证明在实验研究中,如动物研究,以及人类,”鲁齐教授解释说,教授杜兰大学公共卫生与热带医学学院和哈佛T.H.陈公共卫生学院的兼职教授。“最近,全基因组DNA甲基化研究提供了令人信服的数据联系肥胖(即。,BMI, body mass index), likely through a causal pathway.”
许多调查表观遗传变化和肥胖都集中在DNA甲基化,但一些研究调查了其他转录监管机构的影响,如小分子核糖核酸(microrna)肥胖。此外,大多数的工作研究了表观遗传学在人类早期发育的影响。“相信饮食或生活方式的改变更有可能影响外遗传性改变(如DNA甲基化)在发展的窗口,如在产前时期或儿童早期,”齐教授阐述了。“这是可行的,饮食或生活方式的改变也会影响日后肥胖引起的外遗传性改变,但目前缺乏证据。”
所以成年人如何管理自己的体重和肥胖是如何治疗?肥胖的多层的贡献,从个人食物摄取到遗传、表观遗传、代谢营养化妆提倡“个性化”的方法来帮助个人管理体重。”个性化的节食本质上是一个类似的概念精密医学;都强调干预或治疗应该考虑个体差异,这是由内在因素如基因和外遗传性变异,等等,”齐教授解释道。“我认为在未来,我们将能够识别不同的子组的人可能有不同的反应的饮食干预,根据他们的基因组,外遗传性和其他配置文件。在此基础上,精确的干预可能更有效地管理肥胖。”
未来的路线图
我们对疾病的表观遗传学的理解上升推动了一套复杂的表观基因组研究方法。等几乎成了很平常的事亚硫酸氢全基因组测序(WGBS)和甲基化芯片研究DNA甲基化位点,染色质免疫沉淀反应与测序(ChIP-seq)组蛋白修饰使用序列分析为transposase-accessible染色质(ATAC-seq)染色质可访问性,等等。此外,新方法不断出现,包括单细胞技术研究人口的异质性。这种改进的表观基因组学方法分析将有助于揭开表观遗传机制放松管制识别潜在的疾病表观遗传治疗靶点小说,评估药物针对后生放松管制,因此表观遗传疾病的治疗铺平了道路。



