难以集中精力在一个生物LIMS吗?这里是要考虑的基本功能的清单

今年,比以往任何时候都更强调了生物银行提供的关键服务,生物医学研究人员和其他科学家。起生物复杂的操作,管理成千上万,甚至上百万的生物样品和相关科研所需数据。
生物银行面临许多挑战
大多数生物银行面临需要的后勤梦魇收集、运输、处理,存储和船样在不同的地点科学家从许多不同的来源。所有样品和数据必须保持安全贯穿整个过程。此外,生物员工必须管理自己的安全处理生物材料和化学危害,如液态氮。
监管障碍可以特别具有挑战性的生物银行存储样本和数据,称为保护健康信息(φ),从人类的病人。保护隐私的捐助者、生物银行必须遵守不同的监管准则,包括1996年的健康保险携带和责任法案(HIPAA)在美国和欧盟数据保护监管(GDPR) (1、2)。这些指南涵盖生物的许多方面,包括捐赠总经理同意,匿名的样本和临床数据和限制数据访问授权用户。
另一个生物银行所面临的主要挑战是,生物样本热敏,可能受到湿度变化的影响,光和氧含量。因此,生物银行必须建立复杂的基础设施和监控系统维护样本质量。遵循最佳实践指导方针,比如ISO 20387:2018和特色的最佳实践(3、4),生物银行可以确保样品质量仍然很高。
生物银行如何克服这些挑战
通过实现regulatory-compliant、可配置的实验室信息管理系统(LIMS),起生物可以遵循最佳实践指导方针和克服后勤,监管和安全挑战。LIMS可以帮助生物银行规范程序、文档人员培训,并确保工作人员坚持生物验证标准操作程序(sop)。这将最终维持样品质量和完整性以及提高流程效率和人员的安全。
选择合适的生物LIMS系统中
选择一个生物LIMS之前,也被称为生物米资源管理离散元软件、生物经理应该寻找以下特性和功能:
1。管理整个样本的生命周期
LIMS是有效的,它必须能够管理整个样本的生命周期,从收集和捐赠者同意,通过监控运输、处理和存储条件,将样本与临床数据和记录处理样品。LIMS应该整合生物银行使用的自动化系统,如自动存储、温度监测系统或液体处理系统,和更新数据,包括样品存储位置,实时促进互操作性。
2。适应生物的需求
生物员工应该能够创建和配置数据字段在LIMS,包括样本数据、患者数据、样品存储位置和测试结果。
如果一个生物的客户进行多点研究LIMS必须能够协调和集成来自不同数据源的数据。生物银行与多个客户端,LIMS必须能够跟踪和管理样品存储在不同的条件,例如,在-20°C, -80°C或液态氮,为不同的分析和处理,如RNA、DNA或蛋白质化验。此外,LIMS应该能够跟踪和管理遗留/存档样本以及活跃的多个样本的研究,同时保持严格的隐私和安全。
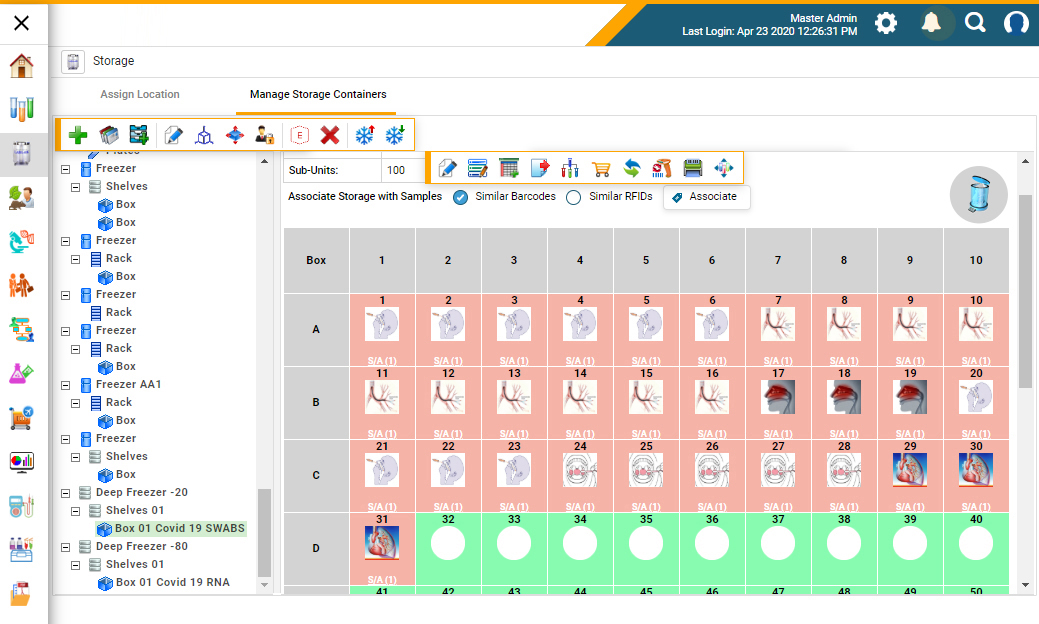
图1:一个生物库管理系统镜像存储生物资料库的库存和定位轻松存储样本(图由CloudLIMS)
3所示。跟踪冻融循环
生物样品温度变化特别敏感,如冻融循环。因此,确保样品质量,至关重要的是,一个生物LIMS跟踪样品储存条件,包括冻融循环,并提醒员工任何温度的偏差。
4所示。符合监管机构的指导方针
生物银行操作在一个严格的监管环境。生物LIMS必须有所有必要的功能符合监管规定。
它必须能够跟踪位置和连锁托管的样本,与用户识别、电子签名和日期和时间戳来提供一个完整的审计跟踪。它还应该提供一个机制来积极管理病人/捐赠者同意和匿名化数据和样本。在美国和欧洲的指南,病人和捐助者必须给自愿、知情同意前生物银行可以使用他们的样品或数据(5、6)。捐助者还必须能够随时撤回,同意。
确保遵守生物管理指南,如ISO 20387:2018、HIPAA和特色的最佳实践,LIMS还可以帮助生物银行管理文件相关的验证流程、标准操作规程和管理员工培训和能力的记录。此外,一个有效的生物LIMS可以帮助安排仪器校准和管理维护数据,确保仪器的保养,对高质量的测试结果是至关重要的。
5。管理数据,确保数据安全
数据管理是法规遵从性的另一个重要组成部分。首先,LIMS必须保留所有病人/捐赠数据安全的数据加密和数据访问控制。只有经过授权的用户可以访问这些信息。提供一个完整的审计跟踪,生物LIMS还必须允许生物银行跟踪所有修订和更改文档和数据,与用户识别和时间和日期戳。
6。是用户友好的,实时更新,并允许可伸缩性
一个生物LIMS应该有一个用户友好的界面,可以但安全,容易搜索。例如,一个基于云的LIMS允许授权用户访问数据,跟踪样品和与合作者共享信息,实时,从任何设备。当结合regulatory-compliant数据安全,这为生物银行提供了一个灵活的方式来管理自己的库存和数据。
最后,应该扩展,允许生物银行LIMS添加更多的样本,更多的客户,更多的用户和更多的网站。

图2:一个示意图表示的基本特征(图由生物软件解决方案CloudLIMS)
结论
生物银行管理大量的挑战性的工作敏感生物样本和大量保护健康数据在一个严格的监管环境。生物LIMS允许生物银行维护样本质量实时监测样本条件在整个样本的生命周期。LIMS也确保法规遵从性通过保持数据安全,限制访问授权用户,提供一个完整的审计跟踪和管理生物文档和人员培训。选择合适的生物信息管理系统,生物经理必须考虑在上述清单中描述的功能。
引用
1。健康保险可移植性和责任法案1996。美国健康与人类服务部。https://aspe.hhs.gov/report/health -保险-可移植性和责任法案- 1996。8月21日,1996年出版。2020年12月22日通过。
2。保罗,美国授权生物银行遵守欧盟GDPR使用基于云的LIMS个人数据保护。CloudLIMS。https://cloudlims.com/lims-posters/empowering-biobanks-to-comply-with-the-eu-gdpr-for-personal-data-protection-using-a-cloud-based-lims.html。10月14日,2019年出版。2020年12月22日通过。
3所示。ISO 20387:2018生物生物技术-生物-一般要求。国际标准化组织。https://www.iso.org/standard/67888.html。2018年8月出版。2020年12月22日通过。
4所示。坎贝尔LD, Astrin JJ, DeSouza Y, et al . 2018年修订的特色最佳实践:更改和编辑团队的开发过程的总结。Biopreservation和生物。2018;16 (1):3 - 6。doi:https://doi.org/10.1089/bio.2018.0001
5。建议厘米/矩形(2016)6部长委员会的成员国在研究人类起源的生物材料。欧洲委员会。https://search.coe.int/cm/Pages/result_details.aspx?ObjectId=090000168064e8ff。2016年出版。2020年12月29日通过。
6。电子的联邦法规。美国政府出版办公室(GPO)https://www.ecfr.gov/cgi-bin/text-idx?m=12&d=18&y=2020&cd=20201223&submit=GO&SID=83cd09e1c0f5c6937cd9d7513160fc3f&node=pt45.1.46&pd=20180719 se45.1.46_1116。12月18日,2020年出版。2020年29日通过。
邵娜莉·保罗是首席运营官CloudLIMS.com



