可视化与配体表达的药物靶点
治疗药品代理,发展的关键是理解和脱靶效应分子可能体内。这些信息使研究人员能够破译代理的作用机理,优化领导候选人,了解副作用以及识别小说用途的药物已经上市。
Cyclica的配体表达®是一个基于云计算平台,屏幕小分子药物与structurally-characterized蛋白质,或“蛋白质组”来确定polypharmacological概要文件。技术识别蛋白质的目标通过利用人工智能和可视化药物对这些目标的影响。随后,科学家们能够识别和非标靶相互作用。我们采访了Naheed Kurji,总裁和首席执行官,安德烈亚斯Windemuth,首席科学官Cyclica找到更多。
劳拉·兰斯顿(LL):为什么要建立一个潜在的治疗目标的确切作用在疾病?你能评论捕捉疾病的临床表现的重要性吗?
Andreas Windemuth Naheed Kurji (NK)和(AW):为了让病人得到最好的标准治疗,药物和治疗代理商必须目标疾病的根源到分子水平。药物相互作用几十甚至上百家蛋白质在人体目标,药物需要用于细胞而不是单个蛋白质的传统范式的目标。复杂的疾病,包括癌症、神经系统疾病和遗传性疾病,需要多个药物,每一个都针对不同的蛋白质,在一个有效的方式一起工作。理解复杂疾病的分子机制可以有效的发展目标蛋白或通路的药物与疾病直接相关。在Cyclica,我们提供了一个端到端启用平台,允许科学家设计,屏幕,个性化药物同时在检查多个目标。这种全面的药物设计方法是至关重要的在创建目标相关的蛋白质在体内的药物,同时避免不良结果。我们同样关注驾驶洞察结构药物基因组学通过合并元素的基因组数据,特别是单核苷酸变异和多态性数据在我们的平台。因此,我们将能够映射物理分子相互作用负责药物反应差异由于遗传变异。这是一个关键的步骤实现精密医学学科发展中治疗患者基于遗传的理解一个特定的疾病。
我:为什么一些更传统的药物发现方法的不足?
NK和亚历山大-伍尔兹:今天,大约需要13年,成本约26.5亿美元给市场带来药物,代表80 x效率下降在过去的50年。根据施et al . 2017自然评论刊物,“最大的贡献者药物研究与开发(R&D)的成本是项目流失率高。磨损是由于各种原因,包括有效性不足、毒性和战略的原因。“高消耗的一个关键原因是,传统的药物发现是专注于设计或筛选最好的药物与一个单一的目标。传统的分子药物设计的建模方法,或者像大规模筛选筛选方法(高温超导)或虚拟筛选(VS),从单个生物目标开始,然后屏幕上图书馆的药物来识别那些与这一目标。虽然这些方法是很有用的,到目前为止他们只需要科学家。现在很好理解,药物与体内许多蛋白质相互作用,一些研究估计30到300个人交互,其中很多都是未知的。虽然狭窄的方法为科学家们提供了一个较短的公认的药物候选列表与已知的目标,它不为他们提供什么大局药物在体内,即其他蛋白质药物被称为其polypharmacology互动。实验方法揭示polypharmacology(如:CETSA或其他质量规范方法)被限制为湿实验室化验可用目标,因此无法规模或发现以前未知的信息。这科技差距Cyclica看到一个机会,就是导致公司的形成和发展的配体表达®。 Recent advancements in applying deep learning to conventional VS through convolutional neural networks (CNN) have emerged as noted by2017年Ragoza等人出现在开源工具,但也提出实质性的担忧的方法。Ragoza等人发现,CNN增强对技术训练的公开数据难以提供价值,因为数据太有限了。在任何情况下,都可用的基于CNN的方法(Ragoza et al ., 2017,瓦拉赫et al ., 2015polypharmacology)地址。
总的来说,制药公司需要一个更快、更便宜的方式来发现和开发更安全、更有效的药物患者的未满足的需求。我们坚信,为了达到这个目标,我们不仅需要加强现有的方法,而且创新的小说,端到端支持技术驱动价值发现管道的多个阶段。重要的是,这些技术必须加强内部工作流程和提高科学家取得更快、更便宜的方式“走”和“不方便”的决定。
会:非标靶相互作用,会产生什么样的影响这些药物发现和开发过程?
NK和亚历山大-伍尔兹:非标靶相互作用本质上是biology-altering与蛋白质相互作用超出了药物的治疗目标,这常常导致意外的和不受欢迎的副作用。传统的target-centric模型如上所述不占这些不相干的相互作用导致成本的增加,时间,和精力。这种现象,药物可能有数百名叫做polypharmacology不相干的交互。一种有毒副作用,在药物发现途径(花费了数亿美元后),会导致巨大的挫折和患者的风险增加。的方法集中在polypharmacology是一个关键转向设计药物以整体的方式通过观察细胞作为一个整体,不只是单一的蛋白质。越来越多的文献表明polypharmacology给定的增加意义的复杂性疾病和意外的相互作用会导致不利影响。在Cyclica计算方法和polypharmacology哲学,提供洞察一个分子的作用机理,探讨了新目标药物项目,重新改现有药物的新适应症(新目标),和设计多靶向药物,解决疾病的光谱在分子水平上。
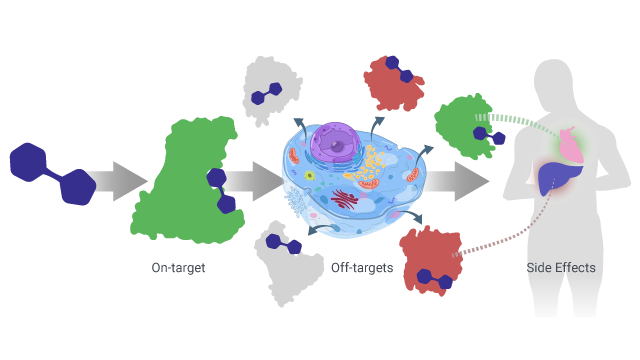
莫莉·坎贝尔(MC):人工智能是如何利用可视化预测药物interactome吗?
NK和亚历山大-伍尔兹:在Cyclica我们坚信人工智能(AI)在药物发现的未来起着至关重要的作用,加速研发创新和提高生产力。AI将科学家与新信息,这样他们就可以加强他们的水平的性能和处理信息的速度。然而,人工智能将不是银弹,当然,它也不会取代科学家。我们相信它是生物物理学和AI将彻底改变药物发现和范式从经典打交互转移到整体细胞药物设计。人工智能是最有用的,当它增强了生物物理学和chemoinformatics方法。我们的云计算平台配体表达被制药公司的科学家来支持他们的努力,并提供一个集成的工作流。通过媒人™,基于结构和AI-augmented权力配体表达技术,科学家可以发现一种药物如何与目标相互作用在分子水平上,人工智能,进一步理解这些数据做出预测调节效果。Cyclica AI是由药物相互作用信息,再加上系统生物学,连接蛋白质功能,疾病,和其他小分子。
司仪:蛋白质组学的发展如何支持Cyclica技术的发展吗?
NK和亚历山大-伍尔兹:蛋白质组学筛选带来一定的挑战,其中大部分是其计算复杂度。然而,过去的几年里,提出了增加计算能力和机器学习算法在很大程度上依赖于现有的知识结合的药物相互作用和提供洞察边际的蛋白质百分比。在Cyclica,我们已经解决了这个问题通过结合计算化学和大数据关注proteome-wide筛查。我们专有的配体表达媒人™技术评估的可能性小分子之间的相互作用和数以千计的蛋白质结构。此前,蛋白质组学筛选的方法被认为是问题由于缺乏蛋白质结构数据。现在,80%的蛋白质结构与之相关的数据和更多的正在以指数速度生成。这个进步的数据,我们可以对所有已知的屏幕小分子结构特点人类蛋白质从而提供一个全面的、整体的了解药物在体内的影响,和对整个蛋白质组和非目标交互。
MC: Cyclica帮助科学家推进领域的药物发现?
NK和亚历山大-伍尔兹:配体表达的平台,一个基于云的、集成的端到端支持平台,制药公司的科学家们使用加速药物发现工作。配体表达的愿景是不可或缺的工具平台的医药研发价值链和以协作的方式支持科学家的工作。我们相信这个集成的工作流将使科学家、生物化学家,医药化学家,等等,关于药物发现做出有效的决策。与科学家一起,我们相信我们的技术可用于了解过多的现有数据。例如,我们已经建立了一个预测ADMET模型集合使用专有的人工智能方法促进小分子药物的翻译。这种技术已经证明提高预测准确性产生ADMET相比传统分类器(阅读更多在这里)。因此,Cyclica的平台,配体表达,预测ADMET技术帮助科学家做出明智的决定从而减少下游成本和潜在风险。
Naheed Kurji和安德烈亚斯Windemuth说劳拉·伊丽莎白·兰斯顿和莫莉坎贝尔科学作家技术网络。188金宝搏备用





