富兰克林湖,新泽西州,2020年7月6日/从/ - BD (Becton, Dickinson和公司)(NYSE: BDX),全球领先的医疗科技公司,今天宣布,美国食品和药物管理局(FDA)批准紧急使用授权(欧洲大学协会)快速、医疗点、SARS-CoV-2诊断测试使用的广泛可用的BD Veritor™+系统。推出这个新试验,结果在一个易于使用的15分钟,高度可移植工具对于改善COVID-19诊断是至关重要的,因为它允许实时搜索结果和决策,而病人仍在现场。
的BD Veritor™系统比手机,目前使用的超过25000家医院,医生办公室,紧急护理中心和零售药店在美国所有50个州。一键功能,工作流的灵活性和易用性使它没有实验室人员设置一个理想的解决方案。它还提供了客户实时报告功能通过BD Synapsys™信息解决方案提供能力容易疾病监测和报告数据监测的目的。
BD是利用其全球制造网络和规模,预计年产能200万年增加测试每周到9月底。该公司已经预计生产1000万测试从7月到9月。
“这将是改变一线医护人员和病人能够访问COVID-19快速诊断测试,提供实时的结果在方便的位置像零售药店,紧急护理中心和医生的办公室,”说戴夫·希双相障碍的综合诊断解决方案。“这样的测试也将帮助社区更明智和更好的准备有助于防止新bet188真人的和额外的一波又一波的峰值COVID-19通过使公共卫生工作者快速识别感染个人和跟踪他们的联系人。具有高度的可移植性,易于使用的即时格式的测试中,大量的测试套件和现有可用,广阔的足迹的BD Veritor™+工具将有助于普遍获得COVID-19检测美国和世界各地的其他国家监管要求。”
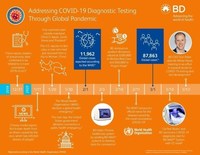
的推出BD Veritor™+ SARS-CoV-2快速检测分析系统是公司的最新努力应对至关重要的卫生需求的综合反应相关的全球大流行。三个分子的新的免疫测定测试连接组合解决方案COVID-19测试已经注册使用BD马克斯™分子系统,包括两个与欧盟配额和两个CE标志。今年迄今为止,该公司为全球卫生保健提供者提供了大约4800万个棉签流感和COVID-19测试,超过285万COVID-19快速分子诊断测试的BD马克斯™系统,和数以百万计的产品用于COVID-19患者的治疗,包括输液泵输液集和导管。
所有BD COVID-19诊断产品市场的监管授权销售。BD打算追求510 (k)间隙BD Veritor™+ SARS-CoV-2化验来自美国食品和药物管理局在稍后的时间。美国消费者对BD COVID-19应该联系诊断解决方案感兴趣IDS.COVIDtests@bd.com。
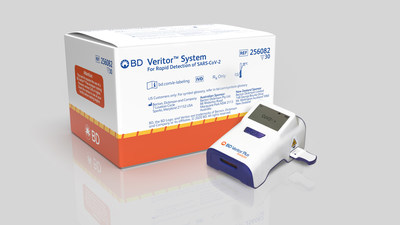
对BD Veritor™SARS-CoV-2化验
的BD Veritor™+ SARS-CoV-2快速检测体系分析被认为是一个CLIA-waived免疫测定设计用于卫生保健机构提供援助在有症状的个体中所扮演的COVID-19快速诊断。BD临床研究执行20多个地点在美国表明,测试能够实现敏感性84%,特异性100%,这符合性能类似的免疫测定为流感A / B测试,RSV,喉炎的症状在BD Veritor™+系统——所有这些都广泛使用,高度相关,临床有效。类似于所有免疫测定测试,FDA建议负面测试结果证实了分子方法确认结果,如有必要,对病人的管理。
BD即时测试没有被清除或FDA批准。测试已经被FDA授权下的欧洲大学协会只检测SARS-CoV-2核衣壳抗原来帮助SARS-CoV-2病毒感染的诊断。它没有被授权使用的检测其他病毒或病菌。测试授权美国申报期间,紧急情况下存在证明授权使用的体外诊断测试检测和/或诊断下的COVID-19 Section 564 (b)(1), 21个事项§360 bbb-3 (b)(1),除非提前终止或撤销授权。
对双相障碍
BD是世界上最大的全球医疗技术公司,是推进世界改善健康的医学发现,诊断和护理的交付。公司支持英雄在前线的医疗发展创新技术,服务和解决方案,帮助推进临床治疗病人和卫生保健提供者的临床过程。BD和其65000名员工有激情和承诺,帮助提高临床医生的安全性和效率的保健交付过程,使实验室科学家能够准确检测疾病和促进研究人员的能力开发下一代的诊断和治疗。BD已经在几乎每一个国家和世界各地的合作伙伴和组织来解决一些最具挑战性的全球卫生问题。通过与客户密切合作,双相障碍可以帮助提高的结果,降低成本,提高效率,改善安全,扩大获得卫生保健。
在双相障碍的更多信息,请访问bd.com。
前瞻性陈述
本新闻稿中包含前瞻性陈述关于利用BD的即时测试和BD的制造能力。前瞻性陈述涉及风险和不确定因素,可能导致实际结果不同物质的表达或暗示的语句,其中许多超出公司的控制,包括风险与市场接受度测试的事件可能会影响我们的制造能力,和其他挑战固有的制造业和商业推出新产品。进一步关于这些风险和不确定性的信息包含在该公司的最新年度报告提交给SEC的备案文件10 - k和其他形式。BD明确声明本文所述的任何这样的声明进行更新,以反映事件或情况在规定的日期之后,除了根据适用的法律或法规。
联系人: |
|
特洛伊柯克帕特里克 |
Monique n Dolecki |
BD公共关系 |
BD投资者关系 |
858.617.2361 |
201.847.5378 |
源BD (Becton, Dickinson和公司)