对精密治疗前列腺癌瀑样创建路径
多机构研究团队由生物工程师领导的调查人员Ankur辛格开发研究工具,揭示一种几乎无法治疗的前列腺癌,打开一个通道,可能导致新的治疗和患者的一线希望。
雄激素受体通路抑制剂可以延长晚期前列腺癌患者的生存。但是大约20%的患者出现神经内分泌晚期前列腺癌在应对这种类型的激素治疗,到目前为止,研究人员还没有有效的方法的研究进展。
“这些患者失去依赖hormone-driven流程和常规治疗不为他们工作,”辛格说,副教授在华莱士·h·库尔特埃默里大学生物医学工程系和佐治亚理工学院和乔治·w·伍德拉夫理工大学机械工程学院。
“没有靶向治疗,所以有明显的临床需要,”他补充道。“但一个主要的挑战是,我们不完全理解这些肿瘤需要什么,什么样的肿瘤微环境,或治疗诱导阻力的因素。没有模型有效地研究这个癌症。”
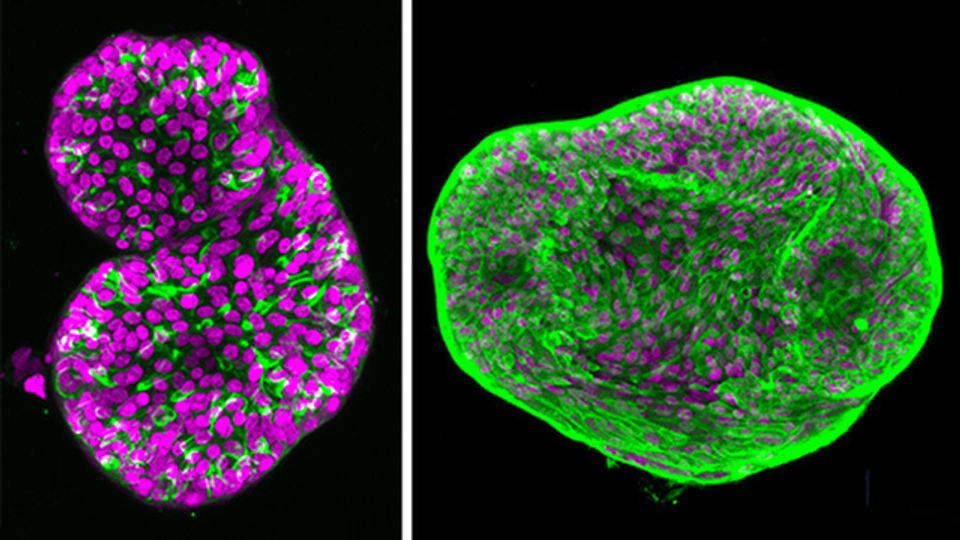
”辛格开始回答这些问题,和他的团队开发了一种前列腺癌瀑样,可以帮助他们模型特定的微环境。它可以提供精密医学向前迈出了重要一步,他们在11月号的《描述先进的材料。
瀑样都很小,三维组织文化从病人的细胞。经过复制不同的人体器官,或模型的疾病。产生完全在体外,瀑样是有价值的工具,研究人员可以在真实的人类micro-anatomies探索有针对性的治疗不伤害病人。
科学家成长瀑样的凝胶作为细胞外基质——富含蛋白质的分子网络,围绕和支持细胞在体内,帮助他们在相互沟通和在多个细胞功能发挥关键作用。
辛格的合作者在这项研究之前开发人工基底膜瀑样神经内分泌前列腺癌模型——也就是说,它们生长细胞在基底膜基质,一个自然的解决方案来自老鼠的肿瘤细胞。使用这些瀑样,研究人员发现了一种新的治疗目标称为EZH2, histone-modifying蛋白质,促进肿瘤的生长。使用一个EZH2抑制剂,他们能够减缓肿瘤的生长。
“EZH2抑制剂可能需要高剂量,我们刚刚开始了解因素控制EZH2的活动。,在某些病人,EZH2抑制剂可能不会消除肿瘤,”辛格说。
推理的EZH2抑制剂将达到全部潜力的肿瘤微环境,他们可以设计——即。,而不是人工基底膜,他们分析了111名患者使用multi-omics活检方法和显微技术彻底这些激进的肿瘤。
他们的发现帮助他们设计和开发合成,Maleimide-polyethyleneglycol-based水凝胶能够准确模拟细胞外基质的肿瘤患者。使用这些瀑样,研究人员可以研究矩阵在肿瘤发展的影响——特别是相关的变化将治疗前列腺癌肿瘤转变为一个无法治愈的。
新瀑样,他们发现,细胞外基质调节EZH2活动和EZH2抑制剂的功效,以前不理解的现象。他们还发现了一个潜在的新的治疗目标,一种名为DRD2的分子。目前,DRD2抑制剂是神经胶质瘤处于临床试验阶段,但他们从来没有测试前列腺神经内分泌肿瘤。
辛格的研究小组发现,某些细胞外基质中发现病人会使神经内分泌肿瘤耐DRD2抑制剂,但阻力可以克服联合治疗:首先,EZH2抑制剂重新编程的细胞,使它们更容易受到DRD2抑制。
“作为单药靶向治疗,DRD2非常令人兴奋,”辛格说,他的合作者包括联合首席调查员Oliver Elemento Englander精密医学研究所主任威尔康奈尔医学,生物医学研究单位和康奈尔大学的医学院。是第一作者马修·Mosquera前博士生辛格的实验室。
辛格认为这项工作可能演变成一个精密医学的新标准。
“不是每个病人的肿瘤微环境是一样的,”辛格说。“我们可以取活检样本,病人的微环境,将特定的信息创建一个瀑样模型,你可以用药物治疗,制定个性化的治疗方案。裁剪这对精密肿瘤是相当巨大的。这是最初的想法。这是最终的目标。”
参考:Mosquera MJ,金正日年代,Bareja R,等人前列腺癌中细胞外基质合成hydrogel-based瀑样调节EZH2和DRD2抑制剂治疗反应。放置板牙。2021年。doi:10.1002 / adma.202100096
本文从以下转载材料。注:材料可能是长度和内容的编辑。为进一步的信息,请联系引用源。



