化学快照和分子图谱与质谱成像
质谱(MS)长期以来一直是化学家工具箱中不可缺少的组成部分,用于鉴定和定量样品中的分子。但是使用质谱作为一种成像技术直到最近二十年才流行起来。
第一次使用质谱成像(MSI,也称为成像质谱或分子成像)是在20世纪90年代,当时范德比尔特大学的Richard Caprioli博士应用基质辅助激光解吸/电离(MALDI)来可视化大鼠组织切片中的肽和蛋白质。1
由于该技术能够在没有抗体的情况下生成组织中生物分子分布的多色化学图,因此迅速引起了制药和临床研究人员的注意。今天,MSI已经在生物制药和医学领域确立了自己作为一种强大的分析方法的地位,其表现就像一个“免疫组织化学的高通量形式,并使发现重要的生物标志物和人类疾病的机制成为可能。
为什么选择MSI?
加拿大英属哥伦比亚维多利亚大学生物化学和微生物学系Christoph Borchers教授认为,MALDI-MSI是首选的组织成像技术,因为它具有更高的多样性和特异性。他解释说,这种方法可以通过两种方式提供绝对的特异性,从而减少误报:
1)对于<1000 Da的分子,可以准确测定分子量(MW)和元素组成。
2)串联质谱可以获得分子的结构信息,它提供了分子特定片段的高分辨率数据。
“如果使用高分辨率的质谱仪,可以同时成像数百到数千个分子,特别是像脂质和代谢物这样的小分子,”Borchers说。
在北美的另一边,在美国新泽西州罗格斯大学新泽西医学院的公共卫生研究所(PHRI), Brendan Prideaux博士正忙着在去欧洲旅行之前完成一项拨款。作为PHRI分析成像中心的质谱师,Prideaux经常使用MSI进行分析现场生物组织内药物和代谢物分布分析。
刚刚发表了一篇评论2在这个问题上,Prideaux告诉我们,MSI比传统的成像技术(如放射自显影)有很大的优势,因为它不依赖于通过添加放射性标签来修饰药物/生物分子。这种在细胞水平的空间细节上直接可视化药物在组织中的分布的能力,不需要标签,使该技术特别适合药物开发的早期阶段。
“我们还可以通过MSI可视化实际分子,而不是追踪放射性标签。我们可以从母体药物的代谢物中分离出母体药物,这是医学研究中的一个关键因素。”
例如,用于治疗结核病的几种基本药物(如吡嗪酰胺)是前药,或药物的非活性形式,需要代谢才能发挥其预期功能。因此,对于研究这些药物功效的研究人员来说,重要的是要确定药物的活性形式(代谢物)是否能到达隐藏在难以到达的区域的细菌群,比如血液供应不足的坏死病灶。
疾病研究中的MSI
到目前为止,MSI的大部分应用已经在癌症诊断领域,特别是对于原位与癌症相关的代谢生物标志物的检测和可视化。在一项外阴癌研究中,MALDI-MSI用于检查三种不同的外阴组织类型。
图像显示细胞角蛋白5 (CK5)在不同组织中的差异表达。3.另一项研究利用MALDI-MSI直接分析培养的人类乳腺细胞系,并绘制可能在浸润性乳腺癌中发挥作用的积累的脂质生物标志物。4
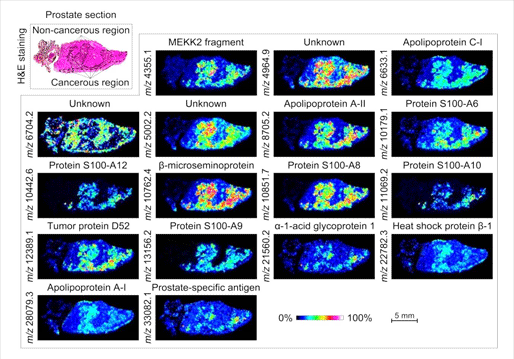
图1所示。MALDI-MS成像人类前列腺癌组织标本癌区和非癌区差异表达蛋白。(图片来源:Borchers等。2016年,J质谱学)。
根据Borchers的说法,MALDI-MSI最重要的突破之一是Caprioli和他的同事发现,“MALDI-MSI可以观察到肿瘤边缘的分子变化,即使组织在组织学上看起来是正常的。”
2010年,Caprioli小组报告说,这些沿组织边缘的变化通常无法通过传统的诊断方法检测到,但MALDI-MS具有特异性和敏感性,可以暴露它们。Caprioli对肾癌活检的研究表明MALDI-MSI可以检测肿瘤微环境的变化。这对癌症手术具有重要意义。5事实上,哈佛大学的琼脂小组现在正在使用MALDI-MS来确定肿瘤的边界。6
在新泽西州的PHRI, Prideaux花了很多时间从事结核病(TB)研究。他一直在使用MALDI-MSI监测结核病药物分布以及疾病进展和/或治疗反应的标志物。他的团队最近开发了一种MALDI-MSI方法,可以同时可视化和绘制肺结核病变内的药物代谢物和细菌脂质生物标志物。7
“使用这种方法不仅表明药物达到了预期的目标,而且表明它正在发挥其预期的效果(或毒理学研究中不希望的效果),”Prideaux解释说。“我们的MALDI-MSI方法使我们能够看到药物与特定细菌目标群体的关系。现在我们正在考虑将这种方法应用于评估药物活性和其他药物诱导的分枝杆菌代谢反应。”
挑战、进步和未来
在Prideaux看来,MSI最具挑战性的一个方面是样品制备。他的团队通过选择紫外线吸收基质和溶剂系统的正确组合开始了他们的MALDI-MSI实验。“药物和基质都应可溶于所使用的溶剂,基质应足够湿润,以便从细胞中提取药物,但又不能太湿,否则可能导致脱位和空间完整性的丧失。”
另一个重大挑战在于对药物分布进行量化。由于脂类和盐类引起的非均相离子抑制,不同细胞/组织类型的药物提取效率不同,以及建立绝对定量标准曲线的困难,很难获得高质量的数据。
“在我们的MSI研究中,我们将检测到的药物信号与标记的标准药物进行标准化,并将其喷在组织表面,”Prideaux说。“这弥补了组织特异性离子抑制,我们可以获得半定量分布图像,其中高浓度药物的组织区域可以清楚地与低浓度区域区分开来。”
在他去年与人合著的一篇评论论文中,Borchers讨论了通过使用新矩阵在MALDI-MSI中取得的最新进展。8“传统基质在检测低分子量肽时经常出现问题,”Borchers解释说。“你在低质量范围内看到高背景信号,在负离子模式下电离效率也很低。但在过去的几年里,我们已经看到了许多高电离效率的MALDI矩阵的发展,矩阵沉积程序,和原位样品处理,以及MS仪器的改进。”
虽然大多数研究使用非靶向MSI,并且只提供组织不同区域的相对浓度,但靶向MSI提供了更高的灵敏度,并且能够绝对定量。Borcher的综述文章提供了提高靶向MSI敏感性的方法,如组织化学衍生化。这些策略与标记的内部标准相结合,使研究人员能够确定每微米这些分子的实际浓度2和/或每个细胞的实际拷贝数,这是临床诊断的重要指标。
总之,Borchers和Prideaux都相信,随着激光光学的进步和质谱仪灵敏度的相应提高,MALDI-MSI的空间分辨能力将继续提高。此外,他们也同意,用于组织药物成像的3D MSI的出现将需要能够处理和处理大型数据集的复杂软件和计算工具。
“随着个性化医疗的潜力不断增长,我希望MSI成为药物发现和开发中多组学方法的一个组成部分,无论是药物定位还是疾病发病机制和治疗反应的生物标志物发现,”Prideaux补充道。
引用:
1 Caprioli, r.m.;农民,t.b.;生物样品的分子成像:利用MALDI-TOF质谱定位多肽和蛋白质。 分析的化学 。 1997 生态学报,69(23),4751-4760。
2普利多,b;Lenaerts, a;质谱法在组织中药物分布的成像和空间分辨定量。咕咕叫。当今。化学。医学杂志。2018, 44, 93-100。
3.张,c;Arentz g;温德鲍姆,L.等。MALDI质谱成像显示,与前体病变分化的外阴上皮内瘤变相比,外阴鳞状细胞癌的CK5水平降低。Int。科学通报;2016, 17。
4王,美国;陈,x;Luan, H.等。基质辅助激光解吸/电离质谱成像细胞培养的脂质组学分析在人乳腺癌侵袭中潜在的脂质标志物。快速Commun。Spectr质量。201630:533 - 542。
5奥本海默,s.r.;Mi, d;桑德斯,m.e.;MALDI质谱法在肾癌肿瘤边缘的分子分析。J.蛋白质组学。2010生态学报,9 (5),2182-2190。
6Calligaris d;费尔德曼博士;诺顿等人。MALDI质谱成像分析垂体腺瘤的近实时肿瘤描绘。美国国家科学促进会,2015生态学报,112(32),9978-9983。
7布兰科,l;Lenaerts, a;Dartois诉;利用MALDI-MS成像技术可视化感染组织中的分枝杆菌生物标志物和结核药物。分析的化学。2018生物医学工程学报,90 (10),6275-6282。
8贝克,t.c.;汉族,j .;Borchers, c.h.,基质辅助激光解吸/电离质谱成像的最新进展。咕咕叫。当今。Biotechnol。2017, 43, 62-69。

